BRCA2 - BRCA2
BRCA2 e BRCA2 ( / ˌ b r æ k ə t U / ) sono un umano gene e la sua proteina di prodotto, rispettivamente. Il simbolo ufficiale (BRCA2, corsivo per il gene, non corsivo per la proteina) e il nome ufficiale (originariamente cancro al seno 2 ; attualmente BRCA2, associato alla riparazione del DNA ) sono mantenuti dal Comitato per la nomenclatura dei geni HUGO . Un simbolo alternativo, FANCD1 , riconosce la sua associazione con ilcomplesso proteico FANC . Gli ortologhi , denominati Brca2 e Brca2, sono comuni in altrespecie di vertebrati . BRCA2 è un gene soppressore del tumore umano(nellospecifico, un gene custode ), presente in tutti gli esseri umani; la sua proteina , chiamata anche dal sinonimo proteina di suscettibilità al cancro al seno di tipo 2 , è responsabile della riparazione del DNA.
BRCA2 e BRCA1 sono normalmente espressi nelle cellule del seno e di altri tessuti, dove aiutano a riparare il DNA danneggiato o a distruggere le cellule se il DNA non può essere riparato. Sono coinvolti nella riparazione del danno cromosomico con un ruolo importante nella riparazione senza errori delle rotture del doppio filamento del DNA . Se BRCA1 o BRCA2 stesso è danneggiato da una mutazione BRCA , il DNA danneggiato non viene riparato correttamente e questo aumenta il rischio di cancro al seno . BRCA1 e BRCA2 sono stati descritti come "geni di suscettibilità al cancro al seno" e "proteine di suscettibilità al cancro al seno". L'allele predominante ha una normale funzione soppressiva del tumore, mentre mutazioni ad alta penetranza in questi geni causano una perdita della funzione soppressiva del tumore, che è correlata ad un aumentato rischio di cancro al seno.
Il gene BRCA2 si trova sul braccio lungo (q) del cromosoma 13 in posizione 12.3 (13q12.3). Il gene di riferimento umano BRCA 2 contiene 27 esoni e il cDNA ha 10.254 paia di basi che codificano per una proteina di 3418 amminoacidi.
Funzione

Sebbene le strutture dei geni BRCA1 e BRCA2 siano molto diverse, almeno alcune funzioni sono correlate. Le proteine prodotte da entrambi i geni sono essenziali per riparare il DNA danneggiato (vedi Figura delle fasi di riparazione ricombinante). BRCA2 lega il DNA a singolo filamento e interagisce direttamente con la ricombinasi RAD51 per stimolare e mantenere l'invasione del filamento, una fase vitale della ricombinazione omologa . La localizzazione di RAD51 alla rottura del doppio filamento del DNA richiede la formazione del complesso BRCA1-PALB2-BRCA2. PALB2 (partner e localizzatore di BRCA2) può funzionare in sinergia con una chimera BRCA2 (denominata piccolo o piBRCA2) per promuovere ulteriormente l'invasione dei filamenti. Queste rotture possono essere causate da radiazioni naturali e mediche o da altre esposizioni ambientali, ma si verificano anche quando i cromosomi si scambiano materiale genetico durante un tipo speciale di divisione cellulare che crea sperma e ovuli ( meiosi ). Le rotture del doppio filamento vengono anche generate durante la riparazione dei collegamenti incrociati del DNA. Riparando il DNA, queste proteine svolgono un ruolo nel mantenere la stabilità del genoma umano e prevenire pericolosi riarrangiamenti genici che possono portare a tumori ematologici e di altro tipo.
BRCA2 ha dimostrato di possedere un ruolo cruciale nella protezione dalla degradazione nucleolitica dipendente da MRE11 delle forcelle invertite che si formano durante lo stallo della forcella di replicazione del DNA (causato da ostacoli come mutazioni, agenti intercalanti ecc.).
Come BRCA1, BRCA2 regola probabilmente l'attività di altri geni e svolge un ruolo critico nello sviluppo dell'embrione.
Significato clinico

Alcune variazioni del gene BRCA2 aumentano i rischi di cancro al seno come parte di una sindrome ereditaria del cancro mammario-ovarico . I ricercatori hanno identificato centinaia di mutazioni nel gene BRCA2, molte delle quali causano un aumento del rischio di cancro. Le mutazioni BRCA2 sono solitamente inserzioni o delezioni di un piccolo numero di coppie di basi del DNA nel gene. Come risultato di queste mutazioni, il prodotto proteico del gene BRCA2 è anormale e non funziona correttamente. I ricercatori ritengono che la proteina BRCA2 difettosa non sia in grado di riparare il danno al DNA che si verifica in tutto il genoma. Di conseguenza, vi è un aumento delle mutazioni dovute alla sintesi di traslezione soggetta a errori oltre il danno non riparato al DNA e alcune di queste mutazioni possono causare la divisione incontrollata delle cellule e la formazione di un tumore.
Le persone che hanno due copie mutate del gene BRCA2 hanno un tipo di anemia di Fanconi . Questa condizione è causata da livelli estremamente ridotti della proteina BRCA2 nelle cellule, che consente l'accumulo di DNA danneggiato. I pazienti con anemia di Fanconi sono soggetti a diversi tipi di leucemia (un tipo di cancro delle cellule del sangue); tumori solidi, in particolare della testa, del collo, della pelle e degli organi riproduttivi; e soppressione del midollo osseo (ridotta produzione di cellule del sangue che porta all'anemia ). Le donne che hanno ereditato un gene BRCA1 o BRCA2 difettoso hanno rischi di cancro al seno e alle ovaie così alti e sembrano così selettivi che molti portatori di mutazioni scelgono di sottoporsi a chirurgia profilattica. Ci sono state molte congetture per spiegare una specificità tissutale così sorprendente. I principali determinanti di dove si verificano i tumori ereditari associati a BRCA1 e BRCA2 sono correlati alla specificità tissutale dell'agente patogeno del cancro, dell'agente che causa l'infiammazione cronica o del cancerogeno. Il tessuto bersaglio può avere recettori per l'agente patogeno, essere esposto selettivamente ad agenti cancerogeni e un processo infettivo. Un deficit genomico innato altera le normali risposte ed esacerba la suscettibilità alla malattia negli organi bersaglio. Questa teoria si adatta anche ai dati per diversi soppressori tumorali oltre BRCA1 o BRCA2. Un grande vantaggio di questo modello è che suggerisce che ci sono alcune opzioni oltre alla chirurgia profilattica.
Oltre al cancro al seno negli uomini e nelle donne, le mutazioni in BRCA2 comportano anche un aumento del rischio di cancro alle ovaie , alle tube di Falloppio , alla prostata e al pancreas . In alcuni studi, le mutazioni nella parte centrale del gene sono state associate a un rischio più elevato di cancro ovarico e a un rischio inferiore di cancro alla prostata rispetto alle mutazioni in altre parti del gene. Diversi altri tipi di cancro sono stati osservati anche in alcune famiglie con mutazioni BRCA2.
In generale, le mutazioni genetiche fortemente ereditarie (comprese le mutazioni in BRCA2) rappresentano solo il 5-10% dei casi di cancro al seno; il rischio specifico di ammalarsi di cancro al seno o di altro tipo per chiunque sia portatore di una mutazione BRCA2 dipende da molti fattori.
Storia
| Il gene BRCA2 è stato scoperto nel 1994.
Il gene è stato clonato per la prima volta dagli scienziati di Myriad Genetics , Endo Recherche, Inc., HSC Research & Development Limited Partnership e University of Pennsylvania . I metodi per diagnosticare la probabilità che un paziente con mutazioni in BRCA1 e BRCA2 si ammalasse di cancro erano coperti da brevetti di proprietà o controllati da Myriad Genetics . Il modello di business di Myriad di offrire esclusivamente il test diagnostico ha portato dagli inizi di Myriad come startup nel 1994 al suo essere una società quotata in borsa con 1200 dipendenti e circa $ 500 milioni di entrate annuali nel 2012; ha anche portato a controversie sui prezzi elevati dei test e l'indisponibilità di seconde opinioni da altri laboratori diagnostici, che a loro volta hanno portato alla storica causa Association for Molecular Pathology contro Myriad Genetics . Mutazioni della linea germinale BRCA2 ed effetto fondatoreTutte le mutazioni della linea germinale BRCA2 identificate fino ad oggi sono state ereditate, suggerendo la possibilità di un ampio effetto "fondatore" in cui una determinata mutazione è comune a un gruppo di popolazione ben definito e può essere teoricamente fatta risalire a un antenato comune. Data la complessità dello screening delle mutazioni per BRCA2, queste mutazioni comuni possono semplificare i metodi necessari per lo screening delle mutazioni in determinate popolazioni. L'analisi delle mutazioni che si verificano con alta frequenza permette anche lo studio della loro espressione clinica. Un esempio lampante di una mutazione capostipite si trova in Islanda, dove una singola mutazione BRCA2 (999del5) rappresenta praticamente tutte le famiglie di cancro al seno/ovarico. Questa mutazione frame-shift porta a un prodotto proteico altamente troncato. In un ampio studio che ha esaminato centinaia di individui affetti da cancro e di controllo, questa mutazione 999del5 è stata trovata nello 0,6% della popolazione generale. Da notare, mentre il 72% dei pazienti che sono risultati portatori aveva una storia familiare moderata o forte di cancro al seno, il 28% aveva poca o nessuna storia familiare della malattia. Ciò suggerisce fortemente la presenza di geni modificanti che influenzano l'espressione fenotipica di questa mutazione, o forse l'interazione della mutazione BRCA2 con fattori ambientali. Ulteriori esempi di mutazioni del fondatore in BRCA2 sono forniti nella tabella seguente.
MeiosiNello stabilimento di Arabidopsis thaliana , la perdita del BRCA2 omologo AtBRCA2 causa gravi difetti sia maschile meiosi e nello sviluppo della femmina gametocyte . La proteina AtBRCA2 è necessaria per la corretta localizzazione della proteina complessa sinaptonemica AtZYP1 e delle ricombinasi AtRAD51 e AtDMC1. Inoltre, AtBRCA2 è necessario per una corretta sinapsi meiotica. Quindi AtBRCA2 è probabilmente importante per la ricombinazione meiotica. Sembra che AtBRCA2 agisca durante la meiosi per controllare le fasi di invasione a singolo filamento mediate da AtRAD51 e AtDMC1 che si verificano durante la riparazione meiotica omologa ricombinante dei danni al DNA. Gli omologhi di BRCA2 sono anche essenziali per la meiosi nel fungo Ustilago maydis , nel verme Caenorhabditis elegans e nel moscerino della frutta Drosophila melanogaster . I topi che producono versioni troncate di BRCA2 sono vitali ma sterili. I ratti mutanti BRCA2 hanno un fenotipo di inibizione della crescita e sterilità in entrambi i sessi. L'aspermatogenesi in questi ratti mutanti è dovuta a un fallimento della sinapsi dei cromosomi omologhi durante la meiosi. Sequenze ripetute BRCDMC1 (DNA meiotic recombinase 1) è unomologo specifico della meiosi di RAD51 che media lo scambio di filamenti durante la riparazione ricombinante omologa . DMC1 promuove la formazione di prodotti di invasione del filamento di DNA (molecole congiunte) tra molecole di DNA omologhe. La DMC1 umana interagisce direttamente con ciascuna di una serie di sequenze ripetute nella proteina BRCA2 (chiamate ripetizioni BRC) che stimolano la formazione di molecole articolari da parte di DMC1. Le ripetizioni BRC sono conformi a un motivo costituito da una sequenza di circa 35 amminoacidi altamente conservati che sono presenti almeno una volta in tutte le proteine simili a BRCA2. Le ripetizioni BRCA2 BRC stimolano la formazione di molecole articolari promuovendo l'interazione del DNA a singolo filamento (ssDNA) con DMC1. Il ssDNA complessato con DMC1 può accoppiarsi con ssDNA omologo da un altro cromosoma durante la fase di sinossi della meiosi per formare una molecola articolare, un passaggio centrale nella ricombinazione omologa . Pertanto, le sequenze ripetute BRC di BRCA2 sembrano svolgere un ruolo chiave nella riparazione ricombinante dei danni al DNA durante la ricombinazione meiotica. Nel complesso, sembra che la ricombinazione omologa durante la meiosi funzioni per riparare i danni al DNA e che BRCA2 svolga un ruolo chiave nell'esecuzione di questa funzione. neurogenesiBRCA2 è richiesto nel topo per la neurogenesi e la soppressione del medulloblastoma . La perdita di ''BRCA2'' colpisce profondamente la neurogenesi, in particolare durante lo sviluppo neurale embrionale e postnatale. Questi difetti neurologici derivano da danni al DNA. Controllo epigeneticoLe alterazioni epigenetiche nell'espressione di BRCA2 (che causano sovraespressione o sottoespressione) sono molto frequenti nei tumori sporadici (vedi Tabella sotto) mentre raramente si riscontrano mutazioni in BRCA2. Nel carcinoma polmonare non a piccole cellule, BRCA2 è epigeneticamente represso dall'ipermetilazione del promotore. In questo caso, l'ipermetilazione del promotore è significativamente associata a bassa espressione di mRNA e bassa espressione di proteine, ma non alla perdita di eterozigosi del gene. Nel cancro ovarico sporadico, si trova un effetto opposto. Il promotore di BRCA2 e le regioni 5'-UTR hanno relativamente pochi o nessun dinucleotidi CpG metilati nel DNA del tumore rispetto a quello del DNA non tumorale e si trova una correlazione significativa tra l'ipometilazione e una sovraespressione di BRCA2 > 3 volte. Ciò indica che l'ipometilazione del promotore BRCA2 e delle regioni 5'-UTR porta alla sovraespressione dell'mRNA di BRCA2. Un rapporto ha indicato un certo controllo epigenetico dell'espressione di BRCA2 da parte dei microRNA miR-146a e miR-148a. Espressione di BRCA2 nel cancroNegli eucarioti , la proteina BRCA2 ha un ruolo importante nella riparazione ricombinante omologa. Nei topi e nell'uomo, BRCA2 media principalmente l'assemblaggio ordinato di RAD51 sul DNA a singolo filamento (ss), la forma attiva per l'accoppiamento omologo e l'invasione del filamento. BRCA2 reindirizza anche RAD51 dal DNA a doppio filamento e previene la dissociazione da ssDNA. Inoltre, i quattro paraloghi di RAD51 , costituiti da RAD51B ( RAD51L1 ), RAD51C (RAD51L2), RAD51D ( RAD51L3 ), XRCC2 formano un complesso chiamato complesso BCDX2 (vedi Figura: Riparazione ricombinante del DNA). Questo complesso partecipa al reclutamento o alla stabilizzazione di RAD51 nei siti di danno. Il complesso BCDX2 sembra agire facilitando l'assemblaggio o la stabilità del filamento nucleoproteico RAD51 . RAD51 catalizza il trasferimento del filamento tra una sequenza rotta e il suo omologo non danneggiato per consentire la risintesi della regione danneggiata (vedi modelli di ricombinazione omologa ). Alcuni studi sui tumori riportano una sovraespressione di BRCA2, mentre altri studi riportano una sottoespressione di BRCA2 . Almeno due rapporti hanno trovato sovraespressione in alcuni tumori sporadici al seno e sottoespressione in altri tumori sporadici al seno. (Vedi la tabella). Molti tumori hanno carenze epigenetiche in vari geni di riparazione del DNA (vedi Frequenze delle epimutazioni nei geni di riparazione del DNA nei tumori ). Queste carenze di riparazione probabilmente causano un aumento dei danni al DNA non riparati. La sovraespressione di BRCA2 osservata in molti tumori può riflettere la sovraespressione compensatoria di BRCA2 e l'aumento della riparazione ricombinante omologa per affrontare almeno parzialmente tali danni al DNA in eccesso. Egawa et al. suggeriscono che l'aumentata espressione di BRCA2 può essere spiegata dall'instabilità genomica frequentemente osservata nei tumori, che induce l'espressione dell'mRNA di BRCA2 a causa di una maggiore necessità di BRCA2 per la riparazione del DNA. La sottoespressione di BRCA2 porterebbe di per sé a un aumento dei danni al DNA non riparati. Errori di replica oltre questi danni (vedi sintesi di traslezione ) porterebbero ad un aumento delle mutazioni e del cancro.
InterazioniBRCA2 ha dimostrato di interagire con Architettura di dominio
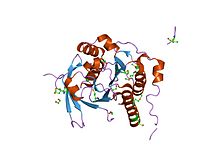
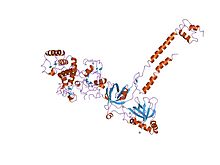
BRCA2 contiene un numero di 39 ripetizioni di amminoacidi che sono fondamentali per il legame a RAD51 (una proteina chiave nella riparazione ricombinante del DNA) e la resistenza al trattamento con metil metansolfonato. Il dominio elicoidale BRCA2 adotta una struttura elicoidale , costituita da un nucleo di cluster a quattro eliche (alfa 1, alfa 8, alfa 9, alfa 10) e due successive forcine beta (da beta 1 a beta 4). Un segmento di circa 50 amminoacidi che contiene quattro eliche corte (da alfa 2 ad alfa 4), si snoda intorno alla superficie della struttura centrale . In BRCA2, le eliche alfa 9 e alfa 10 si impaccano con il dominio BRCA2 OB1 attraverso contatti di van der Waals che coinvolgono residui idrofobici e aromatici, e anche attraverso legami idrogeno a catena laterale e dorsale . Questo dominio lega la proteina DSS1 di 70 aminoacidi (cancellata nella sindrome della mano divisa/piede diviso), che è stata originariamente identificata come uno dei tre geni che mappano su un locus di 1,5 Mb deleto in una sindrome di malformazione dello sviluppo ereditaria. Il dominio BRCA OB1 assume una piega OB, che consiste in un foglio beta a cinque filamenti altamente curvo che si chiude su se stesso per formare un beta-barile . OB1 ha un solco poco profondo formato da una faccia del foglio curvo ed è delimitato da due anelli, uno tra beta 1 e beta 2 e un altro tra beta 4 e beta 5, che consente un debole legame al DNA a singolo filamento . Il dominio lega anche la proteina DSS1 di 70 aminoacidi (cancellata nella sindrome della mano divisa/piede diviso). Il dominio BRCA OB3 assume una piega OB, che consiste in un foglio beta a cinque filamenti altamente curvo che si chiude su se stesso per formare un beta-barile . OB3 ha un solco pronunciato formato da una faccia del foglio curvo ed è delimitato da due anelli, uno tra beta 1 e beta 2 e un altro tra beta 4 e beta 5, che consente un forte legame ssDNA . Il dominio Tower adotta una struttura secondaria costituita da una coppia di lunghe alfa-eliche antiparallele (lo stelo) che supportano un fascio a tre eliche (3HB) alla loro estremità. Il 3HB contiene un motivo elica-giro-elica ed è simile ai domini di legame del DNA delle ricombinasi sito-specifiche batteriche e dei fattori di trascrizione Myb e omeodomini eucariotici . Il dominio Tower ha un ruolo importante nella funzione oncosoppressore di BRCA2 ed è essenziale per un appropriato legame di BRCA2 al DNA. Brevetti, applicazione, contenzioso e controversieUna domanda di brevetto per il gene isolato BRCA1 e le mutazioni che promuovono il cancro, nonché i metodi per diagnosticare la probabilità di contrarre il cancro al seno, è stata depositata dall'Università dello Utah, dal National Institute of Environmental Health Sciences (NIEHS) e da Myriad Genetics nel 1994 ; nel corso dell'anno successivo, Myriad, in collaborazione con altri ricercatori, ha isolato e sequenziato il gene BRCA2 e identificato mutazioni rilevanti, e il primo brevetto BRCA2 è stato depositato negli Stati Uniti da Myriad e dalle altre istituzioni nel 1995. Myriad è il licenziatario esclusivo di questi brevetti e li ha imposti negli Stati Uniti contro i laboratori di diagnostica clinica. Questo modello di business ha portato da Myriad essere una startup nel 1994 ad essere una società quotata in borsa con 1200 dipendenti e circa $ 500 milioni di entrate annuali nel 2012; ha anche portato a controversie sui prezzi elevati e sull'impossibilità di ottenere una seconda opinione da altri laboratori diagnostici, che a sua volta ha portato alla storica causa Association for Molecular Pathology contro Myriad Genetics . I brevetti iniziano a scadere nel 2014. Peter Meldrum, CEO di Myriad Genetics, ha riconosciuto che Myriad ha "altri vantaggi competitivi che potrebbero rendere superflua tale applicazione [di brevetto]" in Europa. Le decisioni legali relative ai brevetti BRCA1 e BRCA2 influenzeranno il campo dei test genetici in generale. Nel giugno 2013, in Association for Molecular Pathology v. Myriad Genetics (n. 12-398), la Corte Suprema degli Stati Uniti ha stabilito all'unanimità che "Un segmento di DNA presente in natura è un prodotto della natura e non è ammissibile al brevetto semplicemente perché è stato isolato ", invalidando i brevetti di Myriad sui geni BRCA1 e BRCA2. Tuttavia, la Corte ha anche ritenuto che la manipolazione di un gene per creare qualcosa che non si trova in natura potrebbe ancora essere ammissibile alla protezione del brevetto. La Corte Federale dell'Australia è giunta alla conclusione opposta, confermando la validità di un brevetto australiano Myriad Genetics sul gene BRCA1 nel febbraio 2013, ma questa decisione è oggetto di ricorso e l'appello includerà l'esame della sentenza della Corte Suprema degli Stati Uniti. RiferimentiUlteriori letture
link esterno
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||