Legante a ponte - Bridging ligand
Nella chimica di coordinazione , un ligando a ponte è un ligando che collega due o più atomi, solitamente ioni metallici. Il legante può essere atomico o poliatomico. Praticamente tutti i composti organici complessi possono fungere da leganti a ponte, quindi il termine è solitamente limitato a piccoli ligandi come gli pseudoalogenuri o a ligandi progettati specificamente per collegare due metalli.
Nel nominare un complesso in cui un singolo atomo fa da ponte tra due metalli, il ligando a ponte è preceduto dalla lettera greca mu, μ , con un numero in pedice che denota il numero di metalli legati al ligando a ponte. μ 2 è spesso indicato semplicemente come μ. Quando si descrivono i complessi di coordinazione bisogna fare attenzione a non confondere μ con ('eta'), che si riferisce all'apticità . I ligandi che non fanno ponte sono chiamati ligandi terminali .
Elenco dei ligandi a ponte
È noto che praticamente tutti i ligandi fanno ponte, ad eccezione delle ammine e dell'ammoniaca . I comuni leganti a ponte includono la maggior parte degli anioni comuni.
| Legante ponte | Nome | Esempio |
|---|---|---|
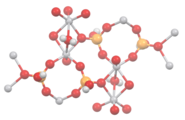
| OH− |
idrossido |
[Fe 2(OH) 2(H 2o) 8] 4+ , vedi olazione |
| O 2- | ossido |
[Cr 2oh 7] 2− , vedi poliossometallato |
| SH− |
idrosolfido |
Cp 2Mo 2(SH) 2S 2 |
| NH− 2 |
amido |
HgNH 2Cl |
| N 3− | nitruro |
[Ir 3N(SO 4) 6(H 2o) 3] 4− , vedi complesso nitridico metallico |
| CO | carbonile |
Fe 2(CO) 9, vedi ponte carbonile |
| Cl− |
cloruro |
Nb 2Cl 10, vedi ligandi ad alogenuri |
| h− |
idruro |
B 2h 6 |
| CN− |
cianuro | ca. Fe 7(CN) 18( blu di prussia ), vedi cianometallato |
| PPh− 2 |
difenilfosfuro | vedi complessi di fosfido dei metalli di transizione |
Molti semplici ligandi organici formano forti ponti tra i centri metallici. Molti esempi comuni includono derivati organici dei suddetti ligandi inorganici (R = alchile, arile): OR−
, SR−
, NR−
2, NR 2− (imido), PR−
2(phosphido, notare l'ambiguità con la voce precedente), PR 2− (phosphinidino), e molti altri.
Esempi
- Composti e complessi con leganti a ponte
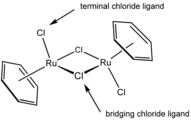
In questo complesso di rutenio ( (benzene)rutenio dicloruro dimero ), due ligandi cloruro sono terminali e due sono μ 2 ponti.
La pirazina è un ligando a ponte in questo composto di dirutenio, chiamato complesso Creutz-Taube .
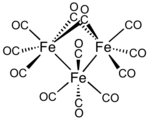
Nel triiron dodecarbonyl , due ligandi CO sono a ponte e dieci sono ligandi terminali. I ligandi di CO terminale e di ponte si scambiano rapidamente.
In NbCl 5 , ci sono due leganti a ponte e otto cloruri terminali.
Il grappolo [Au
6C(PPh
3)
6] 2+ offre un μ 6 - carburo ligando, ma anche qui, il designatore "μ" non è utilizzato di solito.Nel triossido di renio , i ligandi degli ossidi sono tutti μ 2 . Questi ligandi di ossido "incollano" insieme i centri metallici.
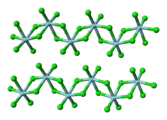
Nel caso di ZrCl
4, ci sono sia ligandi cloruro terminali che a doppio ponte.In rodio (II) acetato , i quattro gruppi acetato colmando ligandi.
legame
Per i ligandi a doppio ponte (μ 2 -), due rappresentazioni limitanti sono le interazioni di legame a 4 e 2 elettroni. Questi casi sono illustrati nella chimica dei gruppi principali da [Me
2Al(μ 2 -Cl)]
2e [Me
2Al(μ 2 -Me)]
2. A complicare questa analisi è la possibilità di un legame metallo-metallo. Studi computazionali suggeriscono che il legame metallo-metallo è assente in molti composti in cui i metalli sono separati da ligandi a ponte. Ad esempio, i calcoli suggeriscono che Fe
2(CO)
9manca di un legame ferro-ferro in virtù di un legame 3-centro 2-elettroni che coinvolge uno dei tre ligandi CO a ponte.
ligandi polifunzionali
I ligandi polifunzionali possono legarsi ai metalli in molti modi e quindi possono collegare i metalli in diversi modi, inclusa la condivisione di un atomo o l'utilizzo di più atomi. Esempi di tali ligandi poliatomici sono gli ossoanioni CO2−
3e i relativi carbossilati , PO3−
4, e i poliossometallati . Sono stati sviluppati diversi ligandi organofosforici che collegano coppie di metalli, un esempio ben noto essendo Ph
2PCH
2PPh
2.
Guarda anche
Riferimenti
- ^ IUPAC , Compendio di terminologia chimica , 2a ed. (il "Libro d'oro") (1997). Versione corretta in linea: (2006-) " legante ponte ". doi : 10.1351/goldbook.B00741
- ^ Unione internazionale di chimica pura e applicata (2005). Nomenclatura della Chimica Inorganica (Raccomandazioni IUPAC 2005). Cambridge (Regno Unito): RSC – IUPAC . ISBN 0-85404-438-8 . pp. 163-165. Versione elettronica.
- ^ Werner, H. (2004). "La via verso il ponte: una nuova modalità di legame di fosfani terziari, arsani e stibani". Angelo. chimica Int. Ed. 43 (8): 938–954. doi : 10.1002/anie.200300627 . PMID 14966876 .
- ^ Koo, H.-J.; Whangbo, M.; VerNooy, PD; Torardi, CC; Marshall, WJ (2002). "Crescita del flusso di vanadil pirofosfato, (VO) 2 P 2 O 7 e analisi del dimero di spin delle interazioni di scambio di spin di (VO) 2 P 2 O 7 e vanadil idrogeno fosfato, VO (HPO 4 ) . 0,5 H 2 O" . Inorg. chimica 41 : 4664-72. doi : 10.1021/ic020249c . PMID 12206689 .
- ^ a b verde, JC; Verde, MLH; Parkin, G. (2012). "La presenza e la rappresentazione di legami a due elettroni a tre centri in composti inorganici covalenti". chimica Comune 2012 : 11481-503. doi : 10.1039/c2cc35304k . PMID 23047247 .