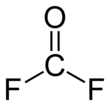
fluoruro di carbonile - Carbonyl fluoride
|
|
|||
| Nomi | |||
|---|---|---|---|
|
Nome IUPAC preferito
Difluoruro di carbonile |
|||
| Altri nomi
fluorofosgene; Ossido di fluoruro di carbonio; Fluorometanoil fluoruro
|
|||
| Identificatori | |||
|
Modello 3D ( JSmol )
|
|||
| ChemSpider | |||
| Scheda informativa ECHA |
100.005.941 |
||
| Numero CE | |||
|
PubChem CID
|
|||
| Numero RTECS | |||
| UNII | |||
| numero ONU | 2417 | ||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Proprietà | |||
| COF 2 | |||
| Massa molare | 66,01 g mol −1 | ||
| Aspetto | Gas incolore | ||
| Densità | 2.698 g / L (gas), 1.139 g / cm 3 (liquido al punto di fusione) | ||
| Punto di fusione | −111,26 ° C (−168,27 ° F; 161,89 K) | ||
| Punto di ebollizione | −84,57 ° C (−120,23 ° F; 188,58 K) | ||
| reagisce violentemente con l'acqua | |||
| Pressione del vapore | 55,4 atm (20°C) | ||
| Struttura | |||
| C 2v | |||
| 0,95 D | |||
| Pericoli | |||
| Principali pericoli | Letale se inalato, reagisce con l'acqua | ||
| Pittogrammi GHS |
   
|
||
| Avvertenza GHS | Pericolo | ||
| H280 , H290 , H314 , H330 , H331 , H370 | |||
| P234 , P260 , P261 , P264 , P270 , P271 , P280 , P284 , P301 + 330 + 331 , P303 + 361 + 353 , P304 + 340 , P305 + 351 + 338 , P307 + 311 , P310 , P311 , P320 , P321 , P363 , P390 , P403 + 233 , P404 , P405 , P410 + 403 , P501 | |||
| NFPA 704 (diamante di fuoco) | |||
| punto d'infiammabilità | Non infiammabile | ||
| NIOSH (limiti di esposizione per la salute negli Stati Uniti): | |||
|
PEL (consentito)
|
nessuna | ||
|
REL (consigliato)
|
TWA 2 ppm (5 mg / m 3 ) ST 5 ppm (15 mg / m 3 ) | ||
|
IDLH (pericolo immediato)
|
ND | ||
| Composti correlati | |||
|
Composti correlati
|
Fosgene carbonile bromuro formil fluoruro Tiocarbonil cloruro Acetone Urea acido carbonico |
||
|
Salvo indicazione contraria, i dati sono forniti per i materiali nel loro stato standard (a 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Riferimenti alla casella informativa | |||
Il fluoruro di carbonile è un composto chimico con la formula COF 2 . Questo gas, come il suo fosgene analogico , è incolore e altamente tossico. La molecola è planare con C 2v simmetria .
Preparazione e proprietà
Il fluoruro di carbonile viene solitamente prodotto come prodotto di decomposizione di idrocarburi fluorurati nella loro decomposizione termica, ad esempio da trifluorometanolo o tetrafluorometano in presenza di acqua:
-
CF
4+ H
2O → COF
2+ 2 HF
Il fluoruro di carbonile può anche essere preparato mediante reazione del fosgene con acido fluoridrico e l'ossidazione del monossido di carbonio , sebbene quest'ultimo tenda a provocare un'eccessiva ossidazione a tetrafluoruro di carbonio . L'ossidazione del monossido di carbonio con difluoruro d'argento è conveniente:
-
CO + 2 AgF
2→ COF
2+ 2 AgF
Il fluoruro di carbonile è instabile in presenza di acqua, idrolizzandosi in anidride carbonica e acido fluoridrico :
-
COF
2+ H
2O → CO
2+ 2 HF
Sicurezza
Il fluoruro di carbonile è tossico con un limite di esposizione raccomandato di 2 ppm come media ponderata nel tempo di 8 ore e 5 ppm come esposizione a breve termine (media di 15 minuti).
Riferimenti
- ^ a b c d e NIOSH Pocket Guide to Chemical Hazards. "# 0108" . Istituto nazionale per la sicurezza e la salute sul lavoro (NIOSH).
- ^ MW Farlow; EH Man; CW Tullock (1960). "Fluoruro di carbonile". Sintesi inorganiche . Sintesi inorganiche. 6 . pagg. 155–158. doi : 10.1002 / 9780470132371.ch48 . ISBN 9780470132371.
- ^ "fluoruro di carbonio" . NIOSH Guida tascabile ai rischi chimici . Centri CDC per il controllo e la prevenzione delle malattie . Estratto il 10/09/2013 .