Cromoforo - Chromophore

Un cromoforo è la parte di una molecola responsabile del suo colore . Il colore che viene visto dai nostri occhi è quello non assorbito dall'oggetto riflettente all'interno di un certo spettro di lunghezze d'onda della luce visibile . Il cromoforo è una regione nella molecola in cui la differenza di energia tra due orbitali molecolari separati rientra nell'intervallo dello spettro visibile. La luce visibile che colpisce il cromoforo può quindi essere assorbita eccitando un elettrone dal suo stato fondamentale in uno stato eccitato . Nelle molecole biologiche che servono a catturare o rilevare l'energia luminosa, il cromoforo è la frazione che provoca un cambiamento conformazionale della molecola quando viene colpita dalla luce.
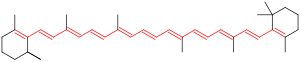
Cromofori del sistema pi-bond coniugato


Proprio come due orbitali p adiacenti in una molecola formeranno un legame pi , tre o più orbitali p adiacenti in una molecola possono formare un sistema pi coniugato . In un sistema pi coniugato, gli elettroni sono in grado di catturare determinati fotoni mentre gli elettroni risuonano lungo una certa distanza degli orbitali p, in modo simile a come un'antenna radio rileva i fotoni lungo la sua lunghezza. Tipicamente, più è coniugato (più lungo) il sistema pi, più lunga è la lunghezza d'onda del fotone che può essere catturata. In altre parole, con ogni doppio legame adiacente aggiunto che vediamo in un diagramma molecolare, possiamo prevedere che il sistema avrà progressivamente più probabilità di apparire giallo ai nostri occhi poiché è meno probabile che assorba la luce gialla e più probabile che assorba la luce rossa. ("I sistemi coniugati di meno di otto doppi legami coniugati assorbono solo nella regione ultravioletta e sono incolori per l'occhio umano", "I composti che sono blu o verdi in genere non si basano solo sui doppi legami coniugati.")
Nei cromofori coniugati , gli elettroni saltano tra livelli energetici che sono orbitali pi estesi , creati da una serie di legami alternati singoli e doppi , spesso nei sistemi aromatici . Esempi comuni includono la retina (utilizzata nell'occhio per rilevare la luce), vari coloranti alimentari , coloranti per tessuti ( composti azoici ), indicatori di pH , licopene , -carotene e antociani . Vari fattori nella struttura di un cromoforo contribuiscono a determinare a quale regione di lunghezza d'onda in uno spettro il cromoforo assorbirà. L'allungamento o l'estensione di un sistema coniugato con più legami insaturi (multipli) in una molecola tenderà a spostare l'assorbimento a lunghezze d'onda più lunghe. Le regole di Woodward-Fieser possono essere utilizzate per approssimare la lunghezza d'onda massima di assorbimento dell'ultravioletto visibile nei composti organici con sistemi pi-bond coniugati.
Alcuni di questi sono cromofori complessi metallici, che contengono un metallo in un complesso di coordinazione con ligandi. Esempi sono la clorofilla , che viene utilizzata dalle piante per la fotosintesi e l' emoglobina , il trasportatore di ossigeno nel sangue degli animali vertebrati. In questi due esempi, un metallo è complessato al centro di un anello macrociclo tetrapirrolico : il metallo è ferro nel gruppo eme (ferro in un anello porfirinico ) dell'emoglobina, o magnesio complessato in un anello tipo cloro nel caso della clorofilla . Il sistema di legame pi altamente coniugato dell'anello del macrociclo assorbe la luce visibile. La natura del metallo centrale può anche influenzare lo spettro di assorbimento del complesso metallo-macrociclo o proprietà come la durata dello stato eccitato. La porzione tetrapirrolica nei composti organici che non è macrociclica ma ha ancora un sistema di legame pi coniugato agisce ancora come cromoforo. Esempi di tali composti includono bilirubina e urobilina , che presentano un colore giallo.
Auxochrome
Un auxocromo è un gruppo funzionale di atomi attaccati al cromoforo che modifica la capacità del cromoforo di assorbire la luce, alterando la lunghezza d'onda o l'intensità dell'assorbimento.
alocromismo
L'alocromismo si verifica quando una sostanza cambia colore al variare del pH . Questa è una proprietà degli indicatori di pH , la cui struttura molecolare cambia al variare di determinate variazioni del pH circostante. Questo cambiamento nella struttura colpisce un cromoforo nella molecola dell'indicatore di pH. Ad esempio, la fenolftaleina è un indicatore di pH la cui struttura cambia al variare del pH, come mostrato nella tabella seguente:
| Struttura | 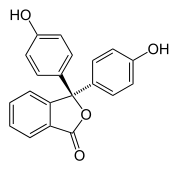 |

|
|---|---|---|
| pH | 0-8.2 | 8.2-12 |
| Condizioni | acido o quasi neutro | di base |
| Nome del colore | incolore | dal rosa al fucsia |
| Colore |
In un intervallo di pH di circa 0-8, la molecola ha tre anelli aromatici tutti legati a un atomo di carbonio ibridizzato sp 3 tetraedrico nel mezzo che non fa coniugare il legame negli anelli aromatici. A causa della loro estensione limitata, gli anelli aromatici assorbono la luce solo nella regione dell'ultravioletto, quindi il composto appare incolore nell'intervallo di pH 0-8. Tuttavia, quando il pH aumenta oltre 8,2, quel carbonio centrale diventa parte di un doppio legame diventando sp 2 ibridato e lasciando un orbitale ap per sovrapporsi al legame negli anelli. Questo fa sì che i tre anelli si coniughino insieme per formare un cromoforo esteso che assorbe la luce visibile a lunghezza d'onda più lunga per mostrare un colore fucsia. A intervalli di pH al di fuori di 0-12, altri cambiamenti della struttura molecolare provocano altri cambiamenti di colore; vedere i dettagli sulla fenolftaleina .
Lunghezze d'onda comuni di assorbimento del cromoforo
| Gruppo funzionale o composto | Lunghezza d'onda di assorbimento |
|---|---|
| Blu di bromofenolo (forma gialla) | 591 nm |
Guarda anche
Riferimenti
link esterno
- Cause del colore : meccanismi fisici mediante i quali viene generato il colore.
- L'elettronica di dimensioni nanometriche ad alta velocità può essere possibile con i cromofori - Azonano.com

