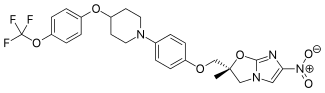
Delamanid - Delamanid
 | |
| Dati clinici | |
|---|---|
| Nomi commerciali | Deltyba |
| Altri nomi | OPC-67683 |
| AHFS / Drugs.com | Informazioni sui farmaci nel Regno Unito |
| Dati di licenza | |
| Vie di somministrazione |
Per via orale ( compresse rivestite con film ) |
| Codice ATC | |
| Stato legale | |
| Stato legale | |
| Dati farmacocinetici | |
| Legame proteico | ≥99,5% |
| Metabolismo | nel plasma dall'albumina, nel fegato dal CYP3A4 (in misura minore) |
| Eliminazione emivita | 30–38 ore |
| Escrezione | non escreto nelle urine |
| Identificatori | |
| |
| Numero CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CheBI | |
| ChEMBL | |
| Cruscotto CompTox ( EPA ) | |
| Dati chimici e fisici | |
| Formula | DO 25 H 25 FA 3 N 4 O 6 |
| Massa molare | 534.492 g·mol −1 |
| Modello 3D ( JSmol ) | |
| |
| |
Delamanid , venduto con il marchio Deltyba , è un farmaco usato per trattare la tubercolosi . Nello specifico viene utilizzato, insieme ad altri farmaci antitubercolari , per la tubercolosi attiva multiresistente . È preso per bocca.
Gli effetti indesiderati comuni includono mal di testa, vertigini e nausea. Altri effetti collaterali includono il prolungamento dell'intervallo QT . Non è stato studiato in gravidanza a partire dal 2016. Delamanid agisce bloccando la produzione di acidi micolici destabilizzando così la parete cellulare batterica . È nella classe di farmaci nitroimidazolo .
Delamanid è stato approvato per uso medico nel 2014 in Europa, Giappone e Corea del Sud. È nell'elenco dei farmaci essenziali dell'Organizzazione mondiale della sanità . A partire dal 2016 la Stop TB Partnership aveva un accordo per ottenere il farmaco per US $ 1.700 ogni sei mesi per l'uso in più di 100 paesi.
Usi medici
Delamanid è usato, insieme ad altri farmaci antitubercolari , per la tubercolosi multiresistente attiva .
Effetti collaterali
Gli effetti indesiderati comuni includono mal di testa, vertigini e nausea. Altri effetti collaterali includono il prolungamento dell'intervallo QT . Non è stato studiato in gravidanza a partire dal 2016.
Interazioni
Delamanid è metabolizzato dall'enzima epatico CYP3A4 ; quindi forti induttori di questo enzima possono ridurne l'efficacia.
Storia
Negli studi clinici di fase II , il farmaco è stato utilizzato in combinazione con trattamenti standard, come quattro o cinque farmaci etambutolo , isoniazide , pirazinamide , rifampicina , antibiotici aminoglicosidici e chinoloni . I tassi di guarigione (misurati come conversione della coltura dell'espettorato ) erano significativamente migliori nei pazienti che assumevano anche delamanid.
L' Agenzia europea per i medicinali (EMA) ha raccomandato l'autorizzazione all'immissione in commercio condizionale per delamanid negli adulti con tubercolosi polmonare multiresistente senza altre opzioni di trattamento a causa della resistenza o della tollerabilità. L'EMA ha considerato che i dati mostrano che i benefici di delamanid superano i rischi, ma che erano necessari ulteriori studi sull'efficacia a lungo termine.
Società e cultura
Il farmaco non era prontamente disponibile a livello globale a partire dal 2015. Si credeva che il prezzo sarebbe stato simile alla bedaquilina , che per sei mesi è di circa 900 dollari nei paesi a basso reddito, 3.000 dollari nei paesi a medio reddito e 30.000 dollari nei paesi ad alto reddito. A partire dal 2016 la Stop TB Partnership aveva un accordo per ottenere il farmaco per US $ 1.700 ogni sei mesi.
Riferimenti
link esterno
- "Delamanide" . Portale informativo sui farmaci . Biblioteca nazionale di medicina degli Stati Uniti.
