Alogenuro arilico - Aryl halide
In chimica organica , un alogenuro arilico (noto anche come haloarene ) è un composto aromatico in cui uno o più atomi di idrogeno, legati direttamente ad un anello aromatico , sono sostituiti da un alogenuro . Gli haloarene sono diversi dagli haloalcani perché presentano molte differenze nei metodi di preparazione e nelle proprietà. I membri più importanti sono i cloruri arilici, ma la classe dei composti è così ampia che esistono molti derivati e applicazioni.
Preparazione
Le due principali vie preparatorie agli alogenuri arilici sono l'alogenazione diretta e i sali di diazonio.
Alogenazione diretta
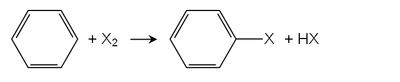
Nella alogenazione Friedel-Crafts , acidi di Lewis servono come catalizzatori. Vengono utilizzati molti cloruri metallici, esempi includono cloruro di ferro (III) o cloruro di alluminio . Il più importante alogenuro arilico, il clorobenzene , viene prodotto per questa via. La monoclorurazione del benzene è sempre accompagnata dalla formazione dei derivati del diclorobenzene.
Gli areni con gruppi donatori di elettroni reagiscono con gli alogeni anche in assenza di acidi di Lewis. Ad esempio, i fenoli e le aniline reagiscono rapidamente con l'acqua di cloro e bromo per dare più prodotti alogenati. La decolorazione dell'acqua di bromo da parte di areni ricchi di elettroni viene utilizzata nel test del bromo .
L'alogenazione diretta degli areni è possibile in presenza di luce o ad alta temperatura. Per i derivati alchilbenzenici, le posizioni alchiliche tendono ad essere alogenate per prime nell'alogenazione dei radicali liberi. Per alogenare l'anello, sono necessari acidi di Lewis e la luce dovrebbe essere esclusa per evitare la reazione concorrente.
Reazioni di Sandmeyer, Balz-Schiemann e Gattermann
La seconda via principale è la reazione di Sandmeyer . Le aniline (aril ammine) vengono convertite nei loro sali di diazonio usando acido nitroso . Ad esempio, il cloruro di rame(I) converte i sali di diazonio in cloruro di arile. Il gas azoto è il gruppo uscente, il che rende questa reazione molto favorevole. La reazione di Schiemann simile utilizza l' anione tetrafluoroborato come donatore di fluoruro. La reazione di Gatterman può anche essere utilizzata per convertire il sale di diazonio in clorobenzene o bromobenzene utilizzando polvere di rame invece di cloruro di rame o bromuro di rame. Ma questo deve essere fatto in presenza rispettivamente di HCl e HBr.
Alogenuri arilici in natura
Gli alogenuri arilici si trovano ampiamente in natura, più comunemente prodotti da organismi marini che utilizzano il cloruro e il bromuro nelle acque oceaniche. Numerosi sono anche i composti aromatici clorurati e bromurati, ad esempio derivati della tirosina, del triptofano e vari derivati del pirrolo. Alcuni di questi alogenuri arilici naturali presentano proprietà medicinali utili.


Tendenze strutturali
Le distanze CX per gli alogenuri arilici seguono l'andamento previsto. Queste distanze per fluorobenzene, clorobenzene, bromobenzene e metil 4-iodobenzoato sono 135,6 (4), 173,90 (23), 189,8 (1) e 209,9 pm , rispettivamente.
reazioni
Sostituzione
A differenza dei tipici alogenuri alchilici, gli alogenuri arilici tipicamente non partecipano alle reazioni di sostituzione convenzionali. Gli alogenuri arilici con gruppi elettron-attrattori nelle posizioni orto e para , possono subire reazioni S N Ar . Ad esempio, il 2,4-dinitroclorobenzene reagisce in soluzione basica per dare un fenolo:
A differenza della maggior parte delle altre reazioni di sostituzione, il fluoruro è il miglior gruppo uscente e lo ioduro il peggiore. Un documento del 2018 indica che questa situazione potrebbe effettivamente essere piuttosto comune, verificandosi in sistemi che in precedenza si presumeva procedessero tramite meccanismi S N Ar.
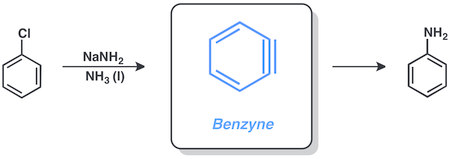
Benzina
Gli alogenuri arilici spesso reagiscono tramite l'intermediazione di benzini . Il clorobenzene e l'ammide sodica reagiscono in ammoniaca liquida per dare anilina attraverso questa via.
Formazione di reagenti organometallici
Gli alogenuri arilici reagiscono con i metalli, generalmente litio o magnesio , per dare più derivati organometallici che funzionano come sorgenti di anioni arilici. Mediante la reazione di scambio metallo-alogeno , gli alogenuri arilici vengono convertiti in composti di aril litio. Illustrativo è la preparazione di fenil litio da bromobenzene utilizzando butil litio (BuLi):
- C 6 H 5 Br + BuLi → C 6 H 5 Li + BuBr
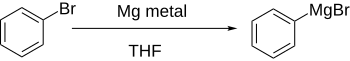
La formazione diretta dei reagenti di Grignard , aggiungendo il magnesio all'alogenuro arilico in una soluzione eterea, funziona bene se l'anello aromatico non è significativamente disattivato da gruppi elettrontrattori.
Altre reazioni
Gli alogenuri possono essere spostati da forti nucleofili tramite reazioni che coinvolgono anioni radicali. In alternativa gli alogenuri arilici, in particolare i bromuri e gli ioduri, subiscono addizione ossidativa , e quindi sono soggetti a reazioni di tipo amminazione di Buchwald-Hartwig .
Il clorobenzene era un tempo il precursore del fenolo , che ora è prodotto dall'ossidazione del cumene . Ad alte temperature, i gruppi arilici reagiscono con l'ammoniaca per dare aniline.
Biodegradazione
Rhodococcus phenolicus è un batterio che degrada il diclorobenzene come unica fonte di carbonio.
Applicazioni
Gli alogenuri arilici prodotti su larga scala sono il clorobenzene e gli isomeri del diclorobenzene. Un'applicazione importante ma interrotta era l'uso del clorobenzene come solvente per disperdere l'erbicida Lasso. Nel complesso, la produzione di cloruri arilici (anche derivati naftil) è in calo dagli anni '80, in parte a causa di preoccupazioni ambientali. La trifenilfosfina è prodotta dal clorobenzene:
- 3 C 6 H 5 Cl + PCl 3 + 6 Na → P(C 6 H 5 ) 3 + 6 NaCl
I bromuri arilici sono ampiamente usati come ritardanti di fiamma. Il membro più importante è il tetrabromobisfenolo-A , che viene preparato per bromurazione diretta del difenolo.