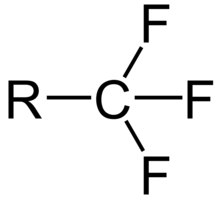
Gruppo trifluorometile - Trifluoromethyl group
Il gruppo trifluorometile è un gruppo funzionale che ha la formula -CF 3 . La denominazione di questo gruppo deriva dal gruppo metilico (che ha la formula -CH 3 ), sostituendo ciascun atomo di idrogeno con un atomo di fluoro . Alcuni esempi comuni sono il trifluorometano H– CF
3, 1,1,1-trifluoroetano H
3C – CF
3e esafluoroacetone F
3C –CO– CF
3. I composti con questo gruppo sono una sottoclasse degli organofluorini .
Proprietà
Il gruppo trifluorometile ha un'elettronegatività significativa che è spesso descritta come intermedia tra le elettronegatività del fluoro e del cloro. Per questo motivo, i composti trifluorometil-sostituiti sono spesso acidi forti, come l' acido trifluorometansolfonico e l'acido trifluoroacetico . Al contrario, il gruppo trifluorometile abbassa la basicità di composti come il trifluoroetanolo .
Usi
Il gruppo trifluorometile si trova in alcuni prodotti farmaceutici, farmaci e composti a base di fluorocarburi naturali sintetizzati abioticamente . L'uso medicinale del gruppo triflorometile risale al 1928, sebbene la ricerca si sia intensificata a metà degli anni '40. Il gruppo trifluorometile viene spesso utilizzato come bioisostero per creare derivati sostituendo un cloruro o un gruppo metilico. Questo può essere utilizzato per regolare le proprietà steriche ed elettroniche di un composto di piombo o per proteggere un gruppo metilico reattivo dall'ossidazione metabolica. Alcuni farmaci notevoli contenenti gruppi trifluorometilici includono efavirenz (Sustiva), un inibitore della trascrittasi inversa dell'HIV; fluoxetina (Prozac), un antidepressivo; e celecoxib (Celebrex), un farmaco antinfiammatorio non steroideo .
Il gruppo trifluorometile può anche essere aggiunto per modificare la solubilità di molecole contenenti altri gruppi di interesse.
Sintesi
Esistono vari metodi per introdurre questa funzionalità. Gli acidi carbossilici possono essere convertiti in gruppi trifluorometilici mediante trattamento con tetrafluoruro di zolfo e composti trialometilici, in particolare trifluorometileteri e trifluorometil aromatici, vengono convertiti in composti trifluorometilici mediante trattamento con trifluoruro di antimonio / pentacloruro di antimonio ( reazione di Swarts ). Un'altra via per gli aromatici trifluorometilici è la reazione degli ioduri arilici con il rame trifluorometilico . Infine, i trifluorometil carbonili possono essere preparati per reazione di aldeidi ed esteri con il reattivo di Ruppert .
Guarda anche
Riferimenti
- ^ Jan E. Vero; T. Darrah Thomas; Rolf W. Inverno; Gary L. Gard (2003). "Elettronegatività da energie di core-ionizzazione: elettronegatività di SF 5 e CF 3 ". Chimica Inorganica . 42 (14): 4437-4441. doi : 10.1021/ic0343298 . PMID 12844318 .
- ^ Yale, Harry L. (1959). "Il gruppo trifluorometile in chimica farmaceutica". Journal of Medicinal and Pharmaceutical Chemistry . 1 (2): 121-133. doi : 10.1021/jm50003a001 . PMID 13665284 .
- ^ GA Olah; Camere RD; GKS Prakash, eds. (1992). Chimica sintetica del fluoro . John Wiley. ISBN 0-471-54370-5.