Acetato di zinco - Zinc acetate

|
|
|
|
| nomi | |
|---|---|
|
nome IUPAC
acetato di zinco
|
|
| Altri nomi
Acido acetico, sale di zinco
Acido acetico, sale di zinco (II) Dicarbomethoxyzinc Zinco diacetate |
|
| Identificatori | |
|
Modello 3D ( JSmol )
|
|
| ChEMBL | |
| ChemSpider | |
| Scheda informativa dell'ECHA |
1000.008.338 |
| E numero | E650 (esaltatore di sapidità) |
|
PubChem CID
|
|
| Numero RTECS | |
| UNII | |
|
Cruscotto CompTox ( EPA )
|
|
|
|
|
|
| Proprietà | |
| Zn(CH 3 COO) 2 (H 2 O) 2 (diidrato) | |
| Massa molare | 219,50 g/mol (diidrato) 183,48 g/mol (anidro) |
| Aspetto | Solido bianco (tutte le forme) |
| Densità | 1,735 g/cm 3 (diidrato) |
| Punto di fusione | Si decompone a 237 ° C (459 ° F; 510 K) (il diidrato perde acqua a 100 ° C) |
| Punto di ebollizione | si decompone |
| 43 g/100 mL (20 °C, diidrato) | |
| solubilità | 1,5 g/100 ml (metanolo) |
| −101.0·10 −6 cm 3 /mol (+2 H 2 O) | |
| Struttura | |
| ottaedrico (diidrato) | |
| tetraedrico | |
| Farmacologia | |
| A16AX05 ( CHI ) | |
| Pericoli | |
| Principali pericoli | leggermente tossico |
| Frasi R (obsolete) | R22 R36 R50/53 |
| Frasi S (obsolete) | S26 S60 S61 |
| Composti correlati | |
|
Altri anioni
|
Cloruro di zinco |
|
Altri cationi
|
Acetato di rame(II) |
|
Composti correlati
|
Acetato di berillio basico |
|
Salvo indicazione contraria, i dati sono forniti per i materiali nel loro stato standard (a 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Riferimenti alla casella informativa | |
L'acetato di zinco è un sale con la formula Zn(CH 3 CO 2 ) 2 , che si presenta comunemente come diidrato Zn(CH 3 CO 2 ) 2 ·2H 2 O. Sia la forma idrata che quella anidra sono solidi incolori che sono stati usati come integratori alimentari. Gli acetati di zinco sono preparati dall'azione dell'acido acetico su carbonato di zinco o metallo di zinco . Quando viene utilizzato come additivo alimentare , ha il numero E E650.
Usi
L'acetato di zinco ha pochi usi a parte le applicazioni dietetiche e medicinali. È stato utilizzato in pastiglie per il trattamento del comune raffreddore . L'acetato di zinco può anche essere usato per trattare le carenze di zinco. Come integratore orale giornaliero viene utilizzato per inibire l'assorbimento del rame da parte dell'organismo come parte del trattamento per la malattia di Wilson . L'acetato di zinco è anche venduto come astringente sotto forma di unguento, lozione topica o combinato con un antibiotico come l' eritromicina per il trattamento topico dell'acne. È comunemente venduto come un unguento topico anti-prurito.
Proprietà e strutture di base
Nell'acetato di zinco anidro lo zinco è coordinato a quattro atomi di ossigeno per dare un ambiente tetraedrico, questi poliedri tetraedrici sono quindi interconnessi da ligandi di acetato per dare una gamma di strutture polimeriche.
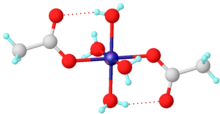
Nell'acetato di zinco diidrato lo zinco è ottaedrico, in cui entrambi i gruppi acetato sono bidentati.
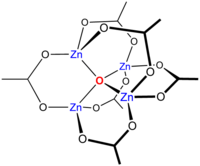
Acetato di zinco basico
Riscaldando Zn(CH 3 CO 2 ) 2 sotto vuoto si ha una perdita di anidride acetica , lasciando un residuo di acetato di zinco basico, di formula Zn 4 O(CH 3 CO 2 ) 6 . Questo composto a grappolo ha la struttura tetraedrica mostrata di seguito. Questa specie assomiglia molto al corrispondente composto di berillio , sebbene sia leggermente espansa con distanze Zn-O ~ 1,97 vs ~ 1,63 per Be 4 O(OAc) 6 .
Guarda anche
- Acetato di berillio basico - isostructural
Riferimenti
- ^ "Zinco - Scheda informativa per gli operatori sanitari" . Office of Dietary Supplements, US National Institutes of Health. 11 febbraio 2016 . Estratto il 15 novembre 2018 .
- ^ Wegmuller, Rita; Tay, Fabiano; Zeder, Christophe; Brnic, Marica; Hurrell, Richard F. (2014). "L'assorbimento dello zinco da parte dei giovani adulti dal citrato di zinco supplementare è paragonabile a quello del gluconato di zinco e superiore a quello dell'ossido di zinco" . Il Giornale della Nutrizione . 144 (2): 132–136. doi : 10.3945/jn.113.181487 . PMC 3901420 . PMID 24259556 .
- ^ "Malattia di Wilson" . NIDDK . Luglio 2014. Archiviato dall'originale il 04-10-2016 . Estratto il 15 novembre 2018 .
- ^ Schachner, L.; Eaglestein, W.; Kittles, C.; Mertz, P. (1990). "Eritromicina topica e terapia con zinco per l'acne". Giornale dell'Accademia americana di dermatologia . 22 (2 Pt 1): 253–60. doi : 10.1016/0190-9622(90)70034-f . PMID 2138176 .
- ^ Clegg, W.; Piccolo, IR; Straughan, BP (15 dicembre 1986). "Acetato di zinco (II) anidro monoclino" . Acta Cristallografica Sezione C . 42 (12): 1701-1703. doi : 10.1107/S010827018609087X .
- ^ Lui, Hongshan (15 novembre 2006). "Un nuovo polimorfo monoclino di acetato di zinco anidro". Acta Cristallografica Sezione E . 62 (12): m3291–m3292. doi : 10.1107/S1600536806046678 .
- ^ Capilla, AV; Aranda, RA (1979). "Acetato di zinco anidro (II) (CH 3 -COO) 2 Zn". Comunicazioni della struttura cristallina . 8 : 795-797.
- ^ van Niekerk, JN; Schoening, FRL; Talbot, JH (10 settembre 1953). "La struttura cristallina dell'acetato di zinco diidrato, Zn (CH3COO) 2.2H2O" . Acta cristallografica . 6 (8): 720-723. doi : 10.1107/S0365110X53002015 .
- ^ Ishioka, T.; Murata, A.; Kitagawa, Y.; Nakamura, KT (15 agosto 1997). "Zinco (II) acetato diidrato". Acta Cristallografica Sezione C . 53 (8): 1029-1031. doi : 10.1107/S0108270197004484 .
- ^ Koyama, H.; Saito, Y. (1954). "La struttura cristallina dell'ossiacetato di zinco, Zn 4 O (CH 3 COO) 6 " . Toro. chimica. Soc. Jpn. 27 (2): 112-114. doi : 10.1246/bcsj.27.112 .