Safranina - Safranin
|
|||

|
|||
|
|||
| Nomi | |||
|---|---|---|---|
|
Nome IUPAC preferito
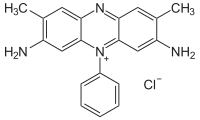
3,7-diammino-2,8-dimetil-5-fenilfenazin-5-ione cloruro |
|||
| Identificatori | |||
|
Modello 3D ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| Scheda informativa ECHA |
100.006.836 |
||
|
PubChem CID
|
|||
| UNII | |||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Proprietà | |||
| C 20 H 19 Cl N 4 | |||
| Massa molare | 350,85 g · mol −1 | ||
| Solubile | |||
| Pericoli | |||
| Pittogrammi GHS |
 
|
||
| Avvertenza GHS | Pericolo | ||
| H315 , H318 | |||
| P264 , P280 , P302 + 352 , P305 + 351 + 338 , P310 , P332 + 313 , P362 | |||
| NFPA 704 (diamante di fuoco) | |||
|
Salvo dove diversamente indicato, i dati sono forniti per i materiali nel loro stato standard (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Riferimenti di Infobox | |||
Safranin (anche Safranin O o basic red 2 ) è un colorante biologico utilizzato in istologia e citologia . La safranina è utilizzata come controcolorante in alcuni protocolli di colorazione, colorando di rosso i nuclei delle cellule . Questa è la classica controcolorazione sia nelle colorazioni di Gram che nella colorazione per endospore . Può anche essere utilizzato per la rilevazione di granuli di cartilagine , mucina e mastociti .
La safranina ha tipicamente la struttura chimica mostrata a destra (a volte descritta come dimetil safranina ). C'è anche trimetil safranina , che ha un gruppo metilico aggiunto nella posizione orto (vedi Arene_substitution_pattern ) dell'anello inferiore. Entrambi i composti si comportano essenzialmente in modo identico nelle applicazioni di colorazione biologica e la maggior parte dei produttori di safranina non fa distinzione tra i due. I preparati commerciali di safranina spesso contengono una miscela di entrambi i tipi.
La safranina è anche usata come indicatore redox nella chimica analitica .
Safranine
Le safranine sono i composti dell'azonio della 2,8-dimetil-3,7-diamminofenazina simmetrica . Sono ottenuti dall'ossidazione congiunta di una molecola di una para- diammina con due molecole di un'ammina primaria ; dalla condensazione di composti para- amminoazo con ammine primarie e dall'azione di para- nitrosodialchilaniline con basi secondarie come difenilmetafenilendiammina. Sono solidi cristallini che mostrano una caratteristica lucentezza metallica verde ; sono facilmente solubili in acqua e si colorano di blu o viola. Sono basi forti e formano sali monacidi stabili . La loro soluzione alcolica mostra una fluorescenza giallo-rossa . La fenosafranina non è molto stabile allo stato libero; il suo cloruro forma placche verdi. Può essere facilmente diazotizzato e il sale di diazonio quando bollito con alcol produce aposafranina o benzene induline, C 18 H 12 N 3 . F. Kehrmann dimostrò che l'aposafranina poteva essere diazotizzata in presenza di acido solforico concentrato freddo , e il sale di diazonio in ebollizione con alcool produceva sali di fenilfenazonio. Aposafranone, C 18 H 12 N 2 O, si forma riscaldando aposafranina con acido cloridrico concentrato . Questi tre composti devono forse essere rappresentati come orto - o come para - chinoni . La "safranina" del commercio è una orto- tolusafranina. La prima sostanza colorante all'anilina ad essere preparata su scala di produzione era la malva , ottenuta da Sir William Henry Perkin riscaldando l'anilina grezza con bicromato di potassio e acido solforico. La mauveina fu convertita in parasafranina (1,8-dimetilsafranina) da Perkin nel 1878 mediante perdita ossidativa / riduttiva del gruppo 7 N - para- tolile. Un'altra safranina ben nota è la fenosafranina (CI 50200, 3,7-diammino-5-fenilfenazinio cloruro) ampiamente utilizzata come colorante istologico, fotosensibilizzatore e sonda redox.
Riferimenti
-
 Questo articolo incorpora il testo di una pubblicazione ora di pubblico dominio : Chisholm, Hugh, ed. (1911). " Safranine ". Encyclopædia Britannica (11 ° ed.). Cambridge University Press.
Questo articolo incorpora il testo di una pubblicazione ora di pubblico dominio : Chisholm, Hugh, ed. (1911). " Safranine ". Encyclopædia Britannica (11 ° ed.). Cambridge University Press.



