Adenosina deaminasi - Adenosine deaminase
| Adenosina/AMP deaminasi | |||||||||
|---|---|---|---|---|---|---|---|---|---|
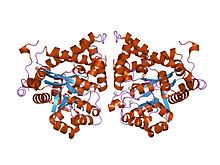 struttura cristallina di plasmodium yoelii adenosina deaminasi (py02076)
| |||||||||
| Identificatori | |||||||||
| Simbolo | A_deaminasi | ||||||||
| Pfam | PF00962 | ||||||||
| Clan Pfam | CL0034 | ||||||||
| InterPro | IPR001365 | ||||||||
| PROSITO | PDOC00419 | ||||||||
| SCOP2 | 1add / SCOPe / SUPFAM | ||||||||
| CDD | cd01320 | ||||||||
| |||||||||
| Dominio dell'adenosina deaminasi (editasi) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificatori | |||||||||
| Simbolo | A_deamin | ||||||||
| Pfam | PF02137 | ||||||||
| InterPro | IPR002466 | ||||||||
| PROSITO | PDOC00419 | ||||||||
| SCOP2 | 1add / SCOPe / SUPFAM | ||||||||
| |||||||||
| Adenosina/AMP deaminasi N-terminale | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificatori | |||||||||
| Simbolo | A_deaminasi_N | ||||||||
| Pfam | PF08451 | ||||||||
| InterPro | IPR013659 | ||||||||
| |||||||||
L'adenosina deaminasi (nota anche come adenosina aminoidrolasi , o ADA ) è un enzima ( EC 3.5.4.4 ) coinvolto nel metabolismo delle purine . È necessario per la scomposizione dell'adenosina dal cibo e per il ricambio degli acidi nucleici nei tessuti.
La sua funzione primaria nell'uomo è lo sviluppo e il mantenimento del sistema immunitario. Tuttavia, il ruolo fisiologico completo dell'ADA non è ancora completamente compreso.
Struttura
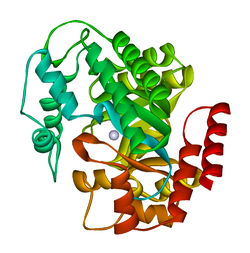
L'ADA esiste sia in forma piccola (come monomero) che in forma grande (come complesso dimero). Nella forma monomerica, l'enzima è una catena polipeptidica, ripiegata in otto filamenti di barili α/β paralleli, che circondano una tasca centrale profonda che è il sito attivo. Oltre alle otto centrali beta botti e otto periferici alfa-eliche , ADA contiene anche cinque eliche supplementari: residui 19-76 volte in tre eliche, situato tra β1 e alfa1 pieghe; e due eliche carbossi-terminali antiparallele si trovano attraverso l'amino-terminale del -barile.
Il sito attivo ADA contiene uno ione zinco, che si trova nel recesso più profondo del sito attivo e coordinato da cinque atomi di His15, His17, His214, Asp295 e del substrato. Lo zinco è l'unico cofattore necessario per l'attività.
Il substrato, l'adenosina, è stabilizzato e legato al sito attivo da nove legami idrogeno. Il gruppo carbossilico di Glu217, grosso modo complanare con l'anello purinico del substrato, è in grado di formare un legame idrogeno con N1 del substrato. Il gruppo carbossilico di Asp296, anch'esso complanare con l'anello purinico del substrato, forma un legame idrogeno con N7 del substrato. Il gruppo NH di Gly184 è in grado di formare un legame idrogeno con N3 del substrato. Asp296 forma legami sia con lo ione Zn 2+ che con 6-OH del substrato. His238 inoltre legami idrogeno al substrato 6-OH. Il 3'-OH del substrato ribosio forma un legame idrogeno con Asp19, mentre il 5'-OH forma un legame idrogeno con His17. Due ulteriori legami idrogeno vengono formati alle molecole d'acqua, all'apertura del sito attivo, dal 2'-OH e 3'-OH del substrato.
A causa dell'arretramento del sito attivo all'interno dell'enzima, il substrato, una volta legato, viene quasi completamente sequestrato dal solvente. L'esposizione superficiale del substrato al solvente quando legato è dello 0,5% dell'esposizione superficiale del substrato allo stato libero.
reazioni
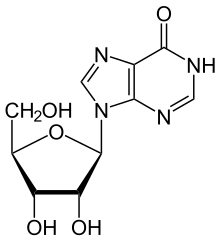
L'ADA deamina irreversibilmente l' adenosina, convertendola nel relativo nucleoside inosina mediante la sostituzione del gruppo amminico con un gruppo cheto.
L'inosina può quindi essere deribosilata (rimossa dal ribosio ) da un altro enzima chiamato purina nucleoside fosforilasi (PNP), convertendola in ipoxantina .
Meccanismo di catalisi
Il meccanismo proposto per la deaminazione catalizzata da ADA è l'eliminazione dell'addizione stereospecifica tramite intermedio tetraedrico. Con entrambi i meccanismi, Zn 2+ come un forte elettrofilo attiva una molecola d'acqua, che viene deprotonata dall'Asp295 di base per formare l'idrossido attaccante. His238 orienta la molecola d'acqua e stabilizza la carica dell'idrossido attaccante. Glu217 è protonato per donare un protone a N1 del substrato.
La reazione è stereospecifica a causa della posizione dei residui di zinco, Asp295 e His238, che sono tutti rivolti verso il lato B dell'anello purinico del substrato.
L'inibizione competitiva è stata osservata per l'ADA, dove il prodotto inosina agisce sull'inibitore competitivo dell'attività enzimatica.
Funzione
L'ADA è considerato uno degli enzimi chiave del metabolismo delle purine. L'enzima è stato trovato in batteri, piante, invertebrati, vertebrati e mammiferi, con un'elevata conservazione della sequenza aminoacidica . L'alto grado di conservazione della sequenza amminoacidica suggerisce la natura cruciale dell'ADA nella via di recupero delle purine.
In primo luogo, l'ADA negli esseri umani è coinvolto nello sviluppo e nel mantenimento del sistema immunitario. Tuttavia, l'associazione dell'ADA è stata osservata anche con la differenziazione delle cellule epiteliali , la neurotrasmissione e il mantenimento della gestazione . È stato anche proposto che l'ADA, oltre alla degradazione dell'adenosina, stimoli il rilascio di amminoacidi eccitatori ed è necessario all'accoppiamento dei recettori dell'adenosina A1 e delle proteine G eterotrimeriche . Il deficit di adenosina deaminasi porta alla fibrosi polmonare, suggerendo che l'esposizione cronica ad alti livelli di adenosina può esacerbare le risposte infiammatorie piuttosto che sopprimerle. È stato anche riconosciuto che la proteina e l'attività dell'adenosina deaminasi sono sovraregolate nei cuori di topo che sovraesprimono HIF1α , il che in parte spiega i livelli attenuati di adenosina nei cuori che esprimono HIF-1α durante lo stress ischemico .
Patologia
Alcune mutazioni nel gene per l'adenosina deaminasi ne impediscono l'espressione. Il deficit risultante è una causa di immunodeficienza combinata grave (SCID), in particolare di trasmissione autosomica recessiva. Livelli carenti di ADA sono stati anche associati a infiammazione polmonare, morte delle cellule timiche e segnalazione difettosa del recettore delle cellule T.
Al contrario, le mutazioni che causano la sovraespressione di questo enzima sono una delle cause dell'anemia emolitica .
Ci sono alcune prove che un allele diverso (ADA2) può portare all'autismo .
Anche livelli elevati di ADA sono stati associati all'AIDS .
isoforme
Esistono 2 isoforme di ADA: ADA1 e ADA2.
- ADA1 si trova nella maggior parte delle cellule del corpo, in particolare linfociti e macrofagi , dove è presente non solo nel citosol e nel nucleo, ma anche come ectoforma sulla membrana cellulare attaccata alla dipeptidil peptidasi-4 (alias CD26). ADA1 è coinvolto principalmente nell'attività intracellulare ed esiste sia in forma piccola (monomero) che in forma grande (dimero). L'interconversione da piccole a grandi forme è regolata da un "fattore di conversione" nel polmone.
- ADA2 è stato identificato per la prima volta nella milza umana. Successivamente è stato trovato in altri tessuti compreso il macrofago dove coesiste con ADA1. Le due isoforme regolano il rapporto tra adenosina e deossiadenosina potenziando l'uccisione dei parassiti. ADA2 si trova prevalentemente nel plasma e nel siero umani ed esiste esclusivamente come omodimero.
Significato clinico
L'ADA2 è la forma predominante presente nel plasma sanguigno umano ed è aumentata in molte malattie, in particolare quelle associate al sistema immunitario: ad esempio l'artrite reumatoide , la psoriasi e la sarcoidosi . Anche l'isoforma plasmatica ADA2 è aumentata nella maggior parte dei tumori. ADA2 non è onnipresente ma coesiste con ADA1 solo nei monociti-macrofagi.
L'ADA plasma totale può essere misurato mediante cromatografia liquida ad alte prestazioni o tecniche enzimatiche o colorimetriche. Forse il sistema più semplice è la misurazione dell'ammoniaca rilasciata dall'adenosina quando viene scomposta in inosina. Dopo incubazione del plasma con una soluzione tamponata di adenosina l'ammoniaca viene fatta reagire con un reattivo di Berthelot per formare un colore blu proporzionato alla quantità di attività enzimatica. Per misurare ADA2, viene aggiunta eritro-9-(2-idrossi-3-nonil) adenina (EHNA) prima dell'incubazione in modo da inibire l'attività enzimatica di ADA1. È l'assenza di ADA1 che causa SCID .
L'ADA può essere utilizzato anche nel workup di versamenti pleurici linfocitari o ascite peritoneale , in quanto tali campioni con bassi livelli di ADA escludono essenzialmente la tubercolosi dalla considerazione.
I versamenti pleurici di tubercolosi possono ora essere diagnosticati con precisione da un aumento dei livelli di adenosina deaminasi nel liquido pleurico, superiore a 40 U per litro.
Cladribina e Pentostatina sono agenti antineoplastici utilizzati nel trattamento della leucemia a cellule capellute ; il loro meccanismo d'azione è l'inibizione dell'adenosina deaminasi.
Guarda anche
Riferimenti
Ulteriori letture
- da Cunha JG (1992). "[Adenosina deaminasi. Un enzima pluridisciplinare]". Acta Médica Portuguesa . 4 (6): 315-23. PMID 1807098 .
- Franco R, Casadó V, Ciruela F, Saura C, Mallol J, Canela EI, Lluis C (luglio 1997). "Superficie cellulare adenosina deaminasi: molto più di un ectoenzima". Progressi in neurobiologia . 52 (4): 283-94. doi : 10.1016/S0301-0082(97)00013-0 . PMID 9247966 . S2CID 40318396 .
- Valenzuela A, Blanco J, Callebaut C, Jacotot E, Lluis C, Hovanessian AG, Franco R (1997). "L'involucro dell'HIV-1 gp120 e le particelle virali bloccano il legame dell'adenosina deaminasi al CD26 umano". Progressi in medicina sperimentale e biologia . 421 : 185-92. doi : 10.1007/978-1-4757-9613-1_24 . ISBN 978-1-4757-9615-5. PMID 9330696 .
- Moriwaki Y, Yamamoto T, Higashino K (ottobre 1999). "Enzimi coinvolti nel metabolismo delle purine - una revisione della localizzazione istochimica e delle implicazioni funzionali". Istologia e istopatologia . 14 (4): 1321–40. PMID 10506947 .
- Hirschhorn R (1993). "Identificazione di due nuove mutazioni missenso (R156C e S291L) in due pazienti ADA-SCID inusuali per la risposta alla terapia con scambi trasfusionali parziali". Mutazione umana . 1 (2): 166-8. doi : 10.1002/humu.138010214 . PMID 1284479 . S2CID 44617309 .
- Berkvens TM, van Ormondt H, Gerritsen EJ, Khan PM, van der Eb AJ (agosto 1990). "Identica delezione 3250 bp tra due ripetizioni AluI nei geni ADA di pazienti ADA-SCID non imparentati". Genomica . 7 (4): 486–90. doi : 10.1016/0888-7543(90)90190-6 . PMID 1696926 .
- Aran JM, Colomer D, Matutes E, Vives-Corrons JL, Franco R (agosto 1991). "Presenza di adenosina deaminasi sulla superficie delle cellule del sangue mononucleate: localizzazione immunochimica mediante microscopia ottica ed elettronica" . Il giornale di istochimica e citochimica . 39 (8): 1001-8. doi : 10.1177/39.8.1856451 . PMID 1856451 .
- Bielat K, Tritsch GL (aprile 1989). "Attività ecto-enzimatica di eritrociti adenosina deaminasi umana". Biochimica molecolare e cellulare . 86 (2): 135-42. doi : 10.1007/BF00222613 . PMID 2770711 . S2CID 20850552 .
- Hirschhorn R, Tzall S, Ellenbogen A, Orkin SH (febbraio 1989). "Identificazione di una mutazione puntiforme risultante in un'adenosina deaminasi (ADA) termolabile in due bambini non imparentati con deficit parziale di ADA" . Il giornale di ricerca clinica . 83 (2): 497-501. doi : 10.1172/JCI113909 . PMC 303706 . PMID 2783588 .
- Murray JL, Perez-Soler R, Bywaters D, Hersh EM (gennaio 1986). "Diminuzione dell'attività dell'adenosina deaminasi (ADA) e 5'nucleotidasi (5NT) nelle cellule T del sangue periferico nella malattia di Hodgkin". Giornale americano di ematologia . 21 (1): 57-66. doi : 10.1002/ajh.2830210108 . PMID 3010705 . S2CID 25540139 .
- Wiginton DA, Kaplan DJ, States JC, Akeson AL, Perme CM, Bilyk IJ, Vaughn AJ, Lattier DL, Hutton JJ (dicembre 1986). "Sequenza completa e struttura del gene per l'adenosina deaminasi umana". Biochimica . 25 (25): 8234-44. doi : 10.1021/bi00373a017 . PMID 3028473 .
- Akeson AL, Wiginton DA, Dusing MR, Stati JC, Hutton JJ (novembre 1988). "Alleli mutanti dell'adenosina deaminasi umana e loro espressione per trasfezione in fibroblasti" . Il giornale di chimica biologica . 263 (31): 16291–6. doi : 10.1016/S0021-9258(18)37591-4 . PMID 3182793 .
- Glader BE, Backer K (febbraio 1988). "Elevata attività dell'adenosina deaminasi dei globuli rossi: un marker di eritropoiesi disordinata nell'anemia di Diamond-Blackfan e altre malattie ematologiche". Giornale britannico di ematologia . 68 (2): 165-8. doi : 10.1111/j.1365-2141.1988.tb06184.x . PMID 3348976 . S2CID 44789636 .
- Petersen MB, Tranebjaerg L, Tommerup N, Nygaard P, Edwards H (febbraio 1987). "Nuova assegnazione del locus del gene dell'adenosina deaminasi al cromosoma 20q13 X 11 mediante studio di un paziente con delezione interstiziale 20q" . Giornale di genetica medica . 24 (2): 93–6. doi : 10.1136/jmg.24.2.93 . PMC 1049896 . PMID 3560174 .
- Orkin SH, Goff SC, Kelley WN, Daddona PE (aprile 1985). "Espressione transitoria di cDNA di adenosina deaminasi umana: identificazione di un clone non funzionale risultante da una singola sostituzione amminoacidica" . Biologia molecolare e cellulare . 5 (4): 762-7. doi : 10.1128/mcb.5.4.762 . PMC 366780 . PMID 3838797 .
- Valerio D, Duyvesteyn MG, Dekker BM, Weeda G, Berkvens TM, van der Voorn L, van Ormondt H, van der Eb AJ (febbraio 1985). "Adenosina deaminasi: caratterizzazione ed espressione di un gene con un promotore notevole" . Il Giornale EMBO . 4 (2): 437-43. doi : 10.1002/j.1460-2075.1985.tb03648.x . PMC 554205 . PMID 3839456 .
- Bonthron DT, Markham AF, Ginsburg D, Orkin SH (agosto 1985). "Identificazione di una mutazione puntiforme nel gene dell'adenosina deaminasi responsabile dell'immunodeficienza" . Il giornale di ricerca clinica . 76 (2): 894-7. doi : 10.1172/JCI112050 . PMC 423929 . PMID 3839802 .
- Daddona PE, Shewach DS, Kelley WN, Argos P, Markham AF, Orkin SH (ottobre 1984). "Deaminasi adenosina umana. cDNA e sequenza completa di aminoacidi primari" . Il giornale di chimica biologica . 259 (19): 12101-6. doi : 10.1016/S0021-9258(20)71325-6 . PMID 6090454 .
- Valerio D, Duyvesteyn MG, Meera Khan P, Geurts van Kessel A, de Waard A, van der Eb AJ (nov 1983). "Isolamento di cloni di cDNA per adenosina deaminasi umana". Gene . 25 (2–3): 231–40. doi : 10.1016/0378-1119(83)90227-5 . PMID 6198240 .
link esterno
- Localizzazione del gene umano ADA nel browser del genoma dell'UCSC .
- Dettagli del gene umano ADA nel browser del genoma UCSC .
- PDBe-KB fornisce una panoramica di tutte le informazioni sulla struttura disponibili nel PDB per l'adenosina deaminasi umana
- PDBe-KB fornisce una panoramica di tutte le informazioni sulla struttura disponibili nel PDB per l'adenosina deaminasi del topo