Ciclobutadiene - Cyclobutadiene
|
|
|||
| Nomi | |||
|---|---|---|---|
|
Nome IUPAC preferito
Cyclobuta-1,3-diene |
|||
| Altri nomi
1,3-ciclobutadiene
ciclobutadiene [4] annulene |
|||
| Identificatori | |||
|
Modello 3D ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
|
PubChem CID
|
|||
| UNII | |||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Proprietà | |||
| C 4 H 4 | |||
| Massa molare | 52,076 g · mol −1 | ||
|
Salvo dove diversamente indicato, i dati sono forniti per i materiali nel loro stato standard (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Riferimenti di Infobox | |||
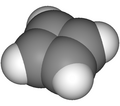
Il ciclobutadiene è un composto organico con la formula C 4 H 4 . È molto reattivo per la sua tendenza a dimerizzare . Sebbene il composto originario non sia stato isolato, alcuni derivati sostituiti sono robusti e una singola molecola di ciclobutadiene è abbastanza stabile. Poiché il composto si degrada mediante un processo bimolecolare , la specie può essere osservata mediante tecniche di isolamento della matrice a temperature inferiori a 35 K. Si ritiene che adotti una struttura rettangolare.
Struttura e reattività
Il composto è l' idrocarburo antiaromatico prototipo con 4 elettroni π. È il più piccolo [ n ] - annulene ([4] -annulene). La sua struttura rettangolare è il risultato dell'effetto Jahn – Teller , che distorce la molecola e ne abbassa la simmetria, convertendo la terzina in uno stato fondamentale di singoletto . Gli stati elettronici del ciclobutadiene sono stati esplorati con una varietà di metodi computazionali . La struttura rettangolare è coerente con l'esistenza di due diversi isomeri di valenza 1,2-dideutero-1,3-ciclobutadiene . Questa distorsione indica che gli elettroni pi sono localizzati, in accordo con la regola di Hückel che prevede che un sistema π di 4 elettroni non è aromatico .
In linea di principio, un'altra situazione è possibile. Vale a dire, il ciclobutadiene potrebbe assumere una geometria quadrata non distorta, se adotta uno stato di spin tripletto . Sebbene sia una possibilità teorica, la forma tripletta del ciclobutadiene genitore e dei suoi derivati sostituiti è rimasta sfuggente per decenni. Tuttavia, nel 2017, lo stato eccitato tripletto quadrato di 1,2,3,4-tetrakis (trimetilsilil) -1,3-ciclobutadiene è stato osservato spettroscopicamente e un gap di tripletto singolo di E ST = 13,9 kcal / mol (o 0,6 eV per molecola) è stata misurata per questo composto.
Sintesi
Diversi derivati del ciclobutadiene sono stati isolati con sostituenti voluminosi sterici . Il tetrakis (terz-butil) ciclobutadiene arancione nasce dalla termolisi del suo isomero tetra-terz-butil tetraedrane . Sebbene il derivato del ciclobutadiene sia stabile (rispetto alla dimerizzazione), si decompone al contatto con O 2 .
Trapping
I campioni di ciclobutadiene sono instabili poiché il composto dimerizza a temperature superiori a 35 K mediante una reazione di Diels-Alder . Sopprimendo le vie di decomposizione bimolecolare, il ciclobutadiene si comporta bene. Così è stato generato in un emicarcefalo . Il composto di inclusione è generato dalla fotodecarbossilazione del biciclopiran-2-one. Quando viene rilasciato dal complesso ospite-ospite, il ciclobutadiene si dimerizza e quindi si converte in cicloottatetraene .
Dopo numerosi tentativi, il ciclobutadiene è stato generato per la prima volta dalla degradazione ossidativa del ciclobutadieneiron tricarbonile con nitrato di ammonio cerio (IV) . Quando viene liberato dal complesso del ferro, il ciclobutadiene reagisce con gli alchini carenti di elettroni per formare un benzene Dewar :
Il benzene Dewar si converte in dimetilftalato per riscaldamento a 90 ° C.
Un derivato del ciclobutadiene è anche accessibile attraverso una cicloaddizione [2 + 2] di un alchino . In questa particolare reazione il reagente di cattura è il 2,3,4,5-tetrafenilciclopenta-2,4-dienone e uno dei prodotti finali (dopo l'espulsione del monossido di carbonio ) è un cicloottatetraene :



![Acetilene-Acetilene [2 + 2] Cycloadditions Chung-Chieh Lee 2006](https://upload.wikimedia.org/wikipedia/commons/thumb/c/c8/CyclobutadienSynthDessyWhite.png/400px-CyclobutadienSynthDessyWhite.png)