chetone - Ketone
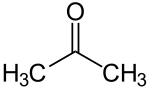
In chimica , un chetone / k Ì t oʊ n / è un gruppo funzionale con la struttura R 2 C = O, dove R può essere una varietà di carbonio contenenti sostituenti . I chetoni contengono un gruppo carbonilico (un doppio legame carbonio-ossigeno). Il chetone più semplice è l' acetone (R = R' = metile ), con la formula CH 3 C(O)CH 3 . Molti chetoni sono di grande importanza in biologia e nell'industria. Gli esempi includono molti zuccheri ( chetosi ), molti steroidi (ad es. testosterone ) e il solvente acetone .
Nomenclatura ed etimologia
La parola chetone deriva da Aketon , un'antica parola tedesca per "acetone".
Secondo le regole della nomenclatura IUPAC , i nomi chetonici sono derivati cambiando il suffisso -ano dell'alcano genitore in -anone . Tipicamente, la posizione del gruppo carbonile è indicata da un numero, ma i nomi tradizionali non sistematici sono ancora generalmente usati per i chetoni più importanti, ad esempio acetone e benzofenone . Questi nomi non sistematici sono considerati nomi IUPAC mantenuti, sebbene alcuni libri di testo introduttivi di chimica utilizzino nomi sistematici come "2-propanone" o "propan-2-one" per il chetone più semplice ( C H 3 -C O -CH 3 ) invece di " acetone".
I nomi derivati dei chetoni si ottengono scrivendo separatamente i nomi dei due gruppi alchilici attaccati al gruppo carbonilico, seguiti da "chetone" come parola separata. I nomi dei gruppi alchilici sono scritti in ordine di complessità crescente: ad esempio, metiletilchetone. Secondo le regole della nomenclatura IUPAC , i gruppi alchilici sono scritti in ordine alfabetico, cioè etilmetilchetone. Quando i due gruppi alchilici sono uguali, il prefisso "di-" viene aggiunto prima del nome del gruppo alchilico. Le posizioni di altri gruppi sono indicate da lettere greche , essendo l'α-carbonio l'atomo adiacente al gruppo carbonilico.
Sebbene usato di rado, oxo è la nomenclatura IUPAC per il gruppo oxo (=O) e viene utilizzato come prefisso quando il chetone non ha la massima priorità. Tuttavia, vengono utilizzati anche altri prefissi. Per alcune sostanze chimiche comuni (principalmente in biochimica), cheto si riferisce al gruppo funzionale chetonico .
Struttura e proprietà

Il carbonio chetone è spesso descritto come " ibridato sp 2 ", descrizione che include sia la loro struttura elettronica che molecolare. I chetoni sono planari trigonali attorno al carbonio chetonico, con angoli di legame C-C-O e C-C-C di circa 120 °. I chetoni differiscono dalle aldeidi in quanto il gruppo carbonilico (CO) è legato a due atomi di carbonio all'interno di uno scheletro di carbonio . Nelle aldeidi, il carbonile è legato a un carbonio e un idrogeno e si trovano alle estremità delle catene di carbonio. I chetoni sono anche distinti da altri gruppi funzionali contenenti carbonile , come acidi carbossilici , esteri e ammidi .
Il gruppo carbonilico è polare perché l'elettronegatività dell'ossigeno è maggiore di quella del carbonio. Pertanto, i chetoni sono nucleofili all'ossigeno ed elettrofili al carbonio. Poiché il gruppo carbonile interagisce con l'acqua mediante legami idrogeno , i chetoni sono in genere più solubili in acqua rispetto ai relativi composti di metilene. I chetoni sono accettori di legami idrogeno. I chetoni di solito non sono donatori di legami a idrogeno e non possono legarsi a idrogeno con se stessi. A causa della loro incapacità di fungere sia da donatori che da accettori di legami idrogeno, i chetoni tendono a non "auto-associarsi" e sono più volatili degli alcoli e degli acidi carbossilici di pesi molecolari comparabili . Questi fattori riguardano la pervasività dei chetoni in profumeria e come solventi.
Classi di chetoni
I chetoni sono classificati in base ai loro sostituenti. Un'ampia classificazione suddivide i chetoni in derivati simmetrici e asimmetrici, a seconda dell'equivalenza dei due sostituenti organici attaccati al centro carbonilico. Acetone e benzofenone (C 6 H 5 C(O) C 6 H 5 ) sono chetoni simmetrici. L'acetofenone (C 6 H 5 C(O)CH 3 ) è un chetone asimmetrico.
dichetoni
Sono noti molti tipi di dichetoni, alcuni con proprietà insolite. Il più semplice è il diacetile (CH 3 C(O)C(O)CH 3 ), un tempo usato come aromatizzante per il burro nei popcorn . Acetilacetone (pentano-2,4-dione) è virtualmente un termine improprio (nome inappropriato) perché questa specie esiste principalmente come monoenolo CH 3 C(O)CH=C(OH)CH 3 . Il suo enolato è un ligando comune nella chimica di coordinazione .
Chetoni insaturi
I chetoni contenenti unità alcheniche e alchiniche sono spesso chiamati chetoni insaturi. Il membro più ampiamente utilizzato di questa classe di composti è il metilvinil chetone , CH 3 C(O)CH=CH 2 , che è utile nella reazione di annullamento di Robinson . Per timore che ci sia confusione, un chetone stesso è un sito di insaturazione; cioè può essere idrogenato .
Chetoni ciclici
Molti chetoni sono ciclici. La classe più semplice ha la formula (CH 2 ) n CO, dove n varia da 2 per il ciclopropanone alle decine. Esistono derivati più grandi. Il cicloesanone, un chetone ciclico simmetrico, è un importante intermedio nella produzione di nylon. L'isoforone , derivato dall'acetone, è un chetone insaturo e asimmetrico che è il precursore di altri polimeri. Il muscone , 3-metilpentadecanone, è un feromone animale . Un altro chetone ciclico è il ciclobutanone , avente la formula C 4 H 6 O.
Tautomerizzazione cheto-enolo
I chetoni che hanno almeno un alfa-idrogeno , subiscono una tautomerizzazione cheto-enolica ; il tautomero è un enolo . La tautomerizzazione è catalizzata sia da acidi che da basi. Di solito, la forma cheto è più stabile dell'enolo. Questo equilibrio consente la preparazione dei chetoni tramite l' idratazione degli alchini .
Proprietà acido/base dei chetoni
I legami CH adiacenti al carbonile nei chetoni sono più acidi ( p K a ≈ 20) rispetto ai legami CH negli alcani (p K a ≈ 50). Questa differenza riflette la stabilizzazione della risonanza dello ione enolato che si forma durante la deprotonazione . L'acidità relativa dell'α-idrogeno è importante nelle reazioni di enolizzazione dei chetoni e di altri composti carbonilici. L'acidità dell'α-idrogeno consente anche ai chetoni e ad altri composti carbonilici di reagire come nucleofili in quella posizione, sia con base stechiometrica che catalitica. Usando basi molto forti come la litio diisopropilamide (LDA, p K a di acido coniugato ~ 36) in condizioni di non equilibrio (-78 ° C, 1,1 equiv LDA in THF, chetone aggiunto alla base), viene generato l' enolato cinetico meno sostituito selettivamente, mentre le condizioni che consentono l'equilibrio (temperatura più elevata, base aggiunta al chetone, utilizzo di basi deboli o insolubili, ad esempio NaOEt in EtOH o NaH) forniscono l' enolato termodinamico più sostituito .
I chetoni sono anche basi deboli, che subiscono protonazione sull'ossigeno carbonilico in presenza di acidi di Brønsted . Gli ioni chetonio (cioè chetoni protonati) sono acidi forti, con valori di p K a stimati tra –5 e –7. Sebbene gli acidi incontrati nella chimica organica siano raramente abbastanza forti da protonare completamente i chetoni, la formazione di concentrazioni all'equilibrio di chetoni protonati è comunque un passo importante nei meccanismi di molte comuni reazioni organiche, come la formazione di un acetale, per esempio. Acidi deboli come il catione piridinio (come si trova nel piridinio tosilato) con un ap K a di 5,2 sono in grado di fungere da catalizzatori in questo contesto, nonostante la costante di equilibrio altamente sfavorevole per la protonazione ( K eq < 10 -10 ).
Caratterizzazione
Un'aldeide differisce da un chetone in quanto ha un atomo di idrogeno attaccato al suo gruppo carbonilico, rendendo le aldeidi più facili da ossidare. I chetoni non hanno un atomo di idrogeno legato al gruppo carbonilico e sono quindi più resistenti all'ossidazione. Sono ossidati solo da potenti agenti ossidanti che hanno la capacità di scindere i legami carbonio-carbonio.
Spettroscopia
I chetoni e le aldeidi assorbono fortemente nello spettro infrarosso vicino a 1700 cm -1 . La posizione esatta del picco dipende dai sostituenti.
Mentre la spettroscopia 1 H NMR non è generalmente utile per stabilire la presenza di un chetone, gli spettri 13 C NMR mostrano segnali in qualche modo a valle di 200 ppm a seconda della struttura. Tali segnali sono tipicamente deboli a causa dell'assenza di effetti nucleari Overhauser . Poiché le aldeidi risuonano a simili spostamenti chimici , vengono impiegati esperimenti di risonanza multipla per distinguere in modo definitivo aldeidi e chetoni.
Test organici qualitativi
I chetoni danno risultati positivi nel test di Brady , la reazione con 2,4-dinitrofenilidrazina per dare il corrispondente idrazone. I chetoni possono essere distinti dalle aldeidi dando esito negativo con il reagente di Tollens o con la soluzione di Fehling . I metilchetoni danno risultati positivi per il test dello iodoformio . I chetoni danno risultati positivi anche se trattati con m- dinitrobenzene in presenza di idrossido di sodio diluito per dare una colorazione viola.
Sintesi
Esistono molti metodi per la preparazione di chetoni su scala industriale e laboratori accademici. I chetoni sono anche prodotti in vari modi dagli organismi; vedere la sezione sulla biochimica di seguito.
Nell'industria, il metodo più importante prevede probabilmente l' ossidazione degli idrocarburi , spesso con aria. Ad esempio, un miliardo di chilogrammi di cicloesanone vengono prodotti ogni anno dall'ossidazione aerobica del cicloesano . L'acetone viene preparato per ossidazione con aria del cumene .
Per applicazioni sintetiche organiche specializzate o su piccola scala , i chetoni vengono spesso preparati mediante ossidazione di alcoli secondari :
- R 2 CH(OH) + O → R 2 C=O + H 2 O
Tipici ossidanti forti (fonte di "O" nella reazione di cui sopra) includono permanganato di potassio o un composto Cr(VI) . Condizioni più miti fanno uso del periodinano di Dess-Martin o dei metodi Moffatt-Swern .
Sono stati sviluppati molti altri metodi, gli esempi includono:
- Per idrolisi degli alogenuri geminali .
- Per idratazione degli alchini . Tali processi avvengono tramite enoli e richiedono la presenza di un acido e HgSO 4 . La successiva tautomerizzazione enol-cheto dà un chetone. Questa reazione produce sempre un chetone, anche con un alchino terminale, l'unica eccezione è l'idratazione dell'acetilene , che produce acetaldeide .
- Da Weinreb Ammidi utilizzando reagenti organometallici stechiometrici.
- I chetoni aromatici possono essere preparati nell'acilazione di Friedel-Crafts , nella relativa reazione di Houben-Hoesch e nel riarrangiamento di Fries .
- L'ozonolisi e le relative sequenze diidrossilazione/ossidative scindono gli alcheni per dare aldeidi o chetoni, a seconda del modello di sostituzione degli alcheni.
- Nel riarrangiamento di Kornblum-DeLaMare i chetoni sono preparati da perossidi e basi.
- Nella ciclizzazione di Ruzicka , i chetoni ciclici sono preparati da acidi dicarbossilici .
- Nella reazione Nef , i chetoni si formano per idrolisi di sali di nitrocomposti secondari .
- Nel giunto Fukuyama , chetoni formano da un tioestere e un composto organozinco.
- Per reazione di un cloruro acido con composti organocadmio o composti organorame .
- La reazione Dakin-West fornisce un metodo efficiente per la preparazione di alcuni metil chetoni da acidi carbossilici.
- I chetoni possono anche essere preparati mediante reazione dei reagenti di Grignard con nitrili , seguita da idrolisi.
- Da decarbossilazione di anidride carbossilica .
- I chetoni possono essere preparati da alochetoni nella dealogenazione riduttiva di alochetoni .
- Nella decarbossilazione chetonica i chetoni simmetrici sono preparati da acidi carbossilici.
- Ossidazione delle ammine con cloruro di ferro (III) .
- Idrolisi di insaturi secondarie ammidi, beta - chetoacido esteri, o p- dichetoni .
- Riarrangiamento acido catalizzato di 1,2-dioli .
reazioni
I chetoni si impegnano in molte reazioni organiche . Le reazioni più importanti derivano dalla suscettibilità del carbonio carbonilico all'addizione nucleofila e dalla tendenza degli enolati ad aggiungersi agli elettrofili. Le addizioni nucleofile includono in ordine approssimativo della loro generalità:
- Con l'acqua (idratazione) dà dioli geminali , che di solito non si formano in quantità apprezzabili (o osservabili)
- Con un acetilide per dare l'α- idrossialchino
- Con l' ammoniaca o un'ammina primaria si ottiene un'immina
- Con l'ammina secondaria si ottiene un'enamine
- Con Grignard e reagenti organolitio per dare, dopo workup acquoso, un alcol terziario
- Con un alcoli o alcossidi per dare l' emichetale o la sua base coniugata. Con un diolo al chetale . Questa reazione è impiegata per proteggere i chetoni.
- Con sodio ammide con conseguente scissione del legame C–C con formazione dell'ammide RCONH 2 e dell'alcano o arene R'H, una reazione chiamata reazione di Haller-Bauer.
- Con forti agenti ossidanti per dare acidi carbossilici .
- Addizione elettrofila , reazione con un elettrofilo dà un catione stabilizzato per risonanza
- Con ilidi di fosfonio nella reazione di Wittig per dare gli alcheni
- Con tioli per dare il tioacetale
- Con idrazina o derivati 1-disostituiti dell'idrazina per dare idrazoni .
- Con un idruro metallico si ottiene un sale alcossido metallico, la cui idrolisi dà l'alcool, esempio di riduzione chetonica
- Con alogeni per formare un α- alochetone , una reazione che procede attraverso un enolo (vedi reazione aloformica )
- Con acqua pesante per dare un chetone α- deuterato
- Frammentazione nella reazione Norrish fotochimica
- Reazione degli 1,4-amminodichetoni agli ossazoli per disidratazione nella sintesi di Robinson-Gabriel
- Nel caso di aril-alchil chetoni, con zolfo e un'ammina danno ammidi nella reazione di Willgerodt
- Con idrossilammina per produrre ossime
- Con agenti riducenti per formare alcoli secondari
- Con perossiacidi per formare esteri nella ossidazione Baeyer-Villiger
Biochimica
I chetoni sono di natura pervasiva. La formazione di composti organici nella fotosintesi avviene tramite il chetone ribulosio-1,5-bisfosfato . Molti zuccheri sono chetoni, noti collettivamente come chetosi . Il chetosio più conosciuto è il fruttosio ; esiste come emichetale ciclico , che maschera il gruppo funzionale chetonico. La sintesi degli acidi grassi avviene tramite chetoni. L'acetoacetato è un intermedio nel ciclo di Krebs che rilascia energia da zuccheri e carboidrati.
In medicina, acetone , acetoacetato e beta-idrossibutirrato sono chiamati collettivamente corpi chetonici , generati da carboidrati , acidi grassi e amminoacidi nella maggior parte dei vertebrati , compresi gli esseri umani. I corpi chetonici sono elevati nel sangue ( chetosi ) dopo il digiuno, inclusa una notte di sonno; sia nel sangue che nell'urina in caso di fame ; in ipoglicemia , dovuta a cause diverse hyperinsulinism ; in vari errori congeniti del metabolismo , e intenzionalmente indotti tramite una dieta chetogenica , e nella chetoacidosi (di solito dovuta a diabete mellito). Sebbene la chetoacidosi sia caratteristica del diabete di tipo 1 scompensato o non trattato , la chetosi o addirittura la chetoacidosi possono verificarsi anche nel diabete di tipo 2 in alcune circostanze.
Applicazioni
I chetoni sono prodotti su larga scala nell'industria come solventi, precursori di polimeri e prodotti farmaceutici. In termini di scala, i chetoni più importanti sono acetone , metiletilchetone e cicloesanone . Sono comuni anche in biochimica, ma meno che nella chimica organica in generale. La combustione degli idrocarburi è un processo di ossidazione incontrollato che dà chetoni e molti altri tipi di composti.
Tossicità
Sebbene sia difficile generalizzare sulla tossicità di una classe così ampia di composti, i chetoni semplici sono, in generale, non altamente tossici. Questa caratteristica è una delle ragioni della loro popolarità come solventi. Eccezioni a questa regola sono le insaturi chetoni come metil vinil chetone con LD 50 di 7 mg / kg (per via orale).
Guarda anche
Riferimenti
link esterno
-
 Mezzi relativi ai chetoni su Wikimedia Commons
Mezzi relativi ai chetoni su Wikimedia Commons