delta -8-Tetraidrocannabinolo - delta-8-Tetrahydrocannabinol
|
|
| nomi | |
|---|---|
|
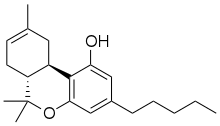
nome IUPAC
6,6,9-trimetil-3-pentil-6a,7,10,10a-tetraidrobenzo[c]cromen-1-olo
|
|
| Altri nomi | |
| Identificatori | |
|
Modello 3D ( JSmol )
|
|
| ChEMBL | |
| ChemSpider | |
| Scheda informativa dell'ECHA |
100.165.076 |
|
PubChem CID
|
|
|
Cruscotto CompTox ( EPA )
|
|
|
|
|
|
| Proprietà | |
| C 21 H 30 O 2 | |
| Massa molare | 314,5 g/mol |
| Densità | 1,0±0,1 g/cm3 |
| Punto di ebollizione | 383,5±42,0 °C |
|
Salvo indicazione contraria, i dati sono forniti per i materiali nel loro stato standard (a 25 °C [77 °F], 100 kPa). |
|
| Riferimenti alla casella informativa | |
Il delta-8-tetraidrocannabinolo ( delta-8-THC , Δ 8 -THC ) è un cannabinoide psicoattivo che si trova nella pianta di Cannabis . È un isomero del delta-9-tetraidrocannabinolo (delta-9-THC, Δ 9 -THC), il composto comunemente noto come THC. ∆ 8 -THC ha proprietà antiemetiche , ansiolitiche , oressigene , analgesiche e neuroprotettive .
Effetti
∆ 8 -THC è moderatamente meno potente di Δ 9 -THC (essendo circa ≈50-66% potente in vivo secondo la maggior parte degli studi scientifici sull'argomento), sebbene i suoi effetti psicologici e fisiologici rimangano qualitativamente simili. Ciò significa essenzialmente che continuerà a medicare/intossicare in modo simile al ∆ 9 -THC, anche se in misura minore per milligrammo di materiale consumato. ∆ 8 -THC può causare aumento della frequenza cardiaca , arrossamento degli occhi , vertigini , secchezza della bocca e della gola, parestesia , tinnito , aumento della consapevolezza del corpo , debolezza , tensione muscolare o tremore , ridotta coordinazione motoria , affaticamento , sonnolenza , alterazioni della vista percezione , immagini visive alterate , miglioramento dei colori o dei contrasti , distorsione del tempo , cambiamenti nella percezione uditiva , euforia , tranquillità , rilassamento , pensieri in corsa , stati introspettivi sognanti o difficoltà nel pensare , parlare , leggere o ricordare .
Uno studio del 1973 che ha testato gli effetti di 8 -THC in cani e scimmie ha riportato che una singola dose orale di 9.000 milligrammi per chilogrammo di massa corporea (mg/kg) non era letale in tutti i cani e le scimmie studiati. Lo stesso studio ha riportato che la dose letale media di 8 -THC nei ratti era paragonabile a quella di ∆ 9 -THC. È stato scoperto che entrambi gli isomeri del THC causano un aumento transitorio della pressione sanguigna nei ratti, sebbene gli effetti dei cannabinoidi sul sistema cardiovascolare siano complessi. Gli studi sugli animali indicano che il 8- THC esercita molti dei suoi effetti centrali legandosi ai recettori dei cannabinoidi presenti in varie regioni del cervello tra cui la corteccia cerebrale , il talamo , i gangli della base , l' ippocampo e il cervelletto .
Farmacologia
Farmacodinamica
Il profilo farmacodinamico di ∆ 8 -THC è simile a quello di ∆ 9 -THC. È un agonista parziale dei recettori cannabinoidi CB 1 e CB 2 con circa la metà della potenza del ∆ 9 -THC nella maggior parte ma non in tutte le misure di attività biologica. È stato riportato che ∆ 8 -THC ha un valore K i di 44 ± 12 nM al recettore CB 1 e 44 ± 17 nM al recettore CB 2 . Questi valori sono superiori a quelli tipicamente riportati per ∆ 9 -THC agli stessi recettori, indicando che ∆ 8 -THC si lega ai recettori dei cannabinoidi in modo meno efficiente rispetto a ∆ 9 -THC.
farmacocinetica
Anche il profilo farmacocinetico di 8 -THC è simile a quello di ∆ 9 -THC. Dopo l'ingestione nell'uomo, gli enzimi epatici del citocromo P450 , inclusi CYP2C9 e CYP3A4, convertono prima il 8 -THC in 11-idrossi-Δ 8 -tetraidrocannabinolo ( 11-OH-Δ 8 -THC ). Successivamente, gli enzimi deidrogenasi convertono 11-OH-Δ 8 -THC in acido 11-nor-Δ 8 -tetraidrocannabinolo-9-carbossilico (11-nor-Δ 8 -THC-9-COOH, noto anche come Δ 8 -THC-11 -acido oico). Infine, l' acido Δ 8 -THC-11-oico subisce la glucuronidazione da parte degli enzimi glucuronidasi per formare il glucuronide dell'acido 11-nor-Δ 8 -tetraidrocannabinol-9-carbossilico (Δ 8 -THC-COOH-glu). Questo prodotto finale viene quindi escreto nelle urine.
Proprietà fisiche e chimiche
∆ 8 -THC è un terpenoide triciclico . Sebbene abbia la stessa formula chimica di ∆ 9 -THC, uno dei suoi doppi legami carbonio-carbonio si trova in una posizione diversa. Questa differenza di struttura aumenta la stabilità chimica del ∆ 8 -THC rispetto al ∆ 9 -THC, allungando la durata di conservazione e consentendo al composto di resistere nel tempo all'ossidazione a cannabinolo . Come altri cannabinoidi, ∆ 8 -THC è molto lipofilo ( log P = 7.4). È un olio estremamente viscoso e incolore a temperatura ambiente.
Mentre ∆ 8 -THC si trova naturalmente nelle piante del genere Cannabis , questo composto può anche essere prodotto in un ambiente industriale o di laboratorio esponendo il CBD ad acidi e calore. I solventi che possono essere utilizzati durante questo processo includono diclorometano , toluene ed esano . Gli acidi che possono essere usati includono acido tosilico , indio (III) triflato , trimetilsilil trifluorometansolfonato , acido cloridrico e acido solforico . Poiché è possibile per i contaminanti chimici da generate durante il processo di conversione CBD Δ 8 THC, come Δ 10 -THC , 9-OH-HHC e altri prodotti secondari, oltre a tutti i reagenti chimici potenzialmente tossici utilizzata durante la produzione , è stata sollevata preoccupazione per la sicurezza dei prodotti 8 -THC non testati o impuri .
∆ 8 -THC ha un doppio legame (a) tra gli atomi di carbonio etichettati con 8 e 9. ∆ 9 -THC ha un doppio legame (a) tra gli atomi di carbonio etichettati con 9 e 10.
La controversia in corso per quanto riguarda lo status giuridico di Δ 8 THC negli Stati Uniti è complicata dalla nomenclatura chimica . Secondo una revisione della letteratura del 2019 pubblicata su Clinical Toxicology , il termine " cannabinoide sintetico " si riferisce tipicamente a un agonista completo dei recettori dei cannabinoidi CB 1 e CB 2 . Secondo la recensione, "Gli effetti psicoattivi (e probabilmente tossici) degli agonisti dei recettori dei cannabinoidi sintetici sono probabilmente dovuti alla loro azione come agonisti completi dei recettori e alla loro maggiore potenza sui recettori CB 1 ". Poiché ∆ 8 -THC e ∆ 9 -THC sono agonisti parziali dei recettori dei cannabinoidi, piuttosto che agonisti completi, questi composti sono meno potenti e meno tossici di molti cannabinoidi sintetici. Sebbene non sia stato definitivamente dimostrato se il pieno agonismo sia la ragione della tossicità, poiché è stato dimostrato che il Delta-9-THC agisce come un completo agonista CB1 su specifici recettori CB1 situati nella sezione dell'ippocampo del cervello. e il cannabinoide sintetico EG-018 agisce come un agonista parziale La classica classe di farmaci a struttura dibenzopiranica dei cannabinoidi che include il THC interagiscono con un punto diverso all'interno del recettore CB1 rispetto ai composti cannabinoidi sintetici di classi chimiche non correlate come i naftoilindoli che possono contribuire alla tossicità .
Storia
La sintesi parziale di Δ 8 THC è stato pubblicato nel 1941 da Roger Adams e colleghi presso l' Università dell'Illinois . Nel 1942, lo stesso gruppo di ricerca ha studiato i suoi effetti fisiologici e psicoattivi dopo somministrazione orale in volontari umani. Le sintesi totali di 8 -THC furono raggiunte nel 1965. Nel 1966, la struttura chimica di ∆ 8 -THC isolata dalla cannabis fu caratterizzata utilizzando metodi moderni da Richard L. Hively, William A. Mosher e Friedrich W. Hoffmann all'Università del Delaware . Una sintesi stereospecifica di ∆ 8 -THC da olivetol e verbenol è stata segnalata da Raphael Mechoulam e colleghi del Weizmann Institute of Science nel 1967. ∆ 8 -THC è stato spesso indicato come "Delta-6-THC" (Δ 6 -THC) nella prima letteratura scientifica, ma questo nome non è più convenzionale tra la maggior parte degli autori.
Società e cultura
Da quando la legge agricola degli Stati Uniti del 2018 è stata firmata nel dicembre 2018, ∆ 8 prodotti di THC parzialmente sintetizzati da fonti conformi (tra cui canapa industriale ed estratti di cannabidiolo derivati ) sono stati venduti da una serie di venditori digitali e una gamma più limitata di mattoni e rivenditori di malta , compresi i negozi di testa . Che vanno da grandi quantità di distillato non raffinato a edibili preparati e cartucce di atomizzatori imbevuti di terpeni derivati dalla cannabis , di solito sono commercializzati come alternative legali federali alle loro controparti ∆ 9 -THC. Tuttavia, lo status legale di ∆ 8 -THC a livello federale è in discussione con alcuni che credono che il DEA IFR di ottobre 2020 si rivolga ai "sintetici" applicati al Delta-8 e ad altri derivati della canapa consentiti dal Farm Bill.
A partire dalla fine del 2020, ∆ 8 -THC ha iniziato ad attirare l'attenzione di molti consumatori di cannabis negli Stati Uniti. Pensato come un'alternativa al tradizionale uso di cannabis, specialmente nelle aree in cui la marijuana è illegale, la notizia di ∆ 8 -THC si è diffusa rapidamente tramite agenzie di stampa, pubblicazioni di cannabis, blog e podcast che hanno attirato una tempesta di attenzione sui social media.
Poiché la commercializzazione di prodotti ∆ 8 -THC non richiede licenze speciali o, nella maggior parte degli stati, analisi chimiche, il fatto che questi prodotti possano essere prodotti e commercializzati a livello nazionale anziché uno stato alla volta e non hanno più tasse di una vendita ordinaria tassa , se ciò, significa che sono molto più economici dei prodotti ∆ 9- THC acquistati in un dispensario di cannabis . Possono essere spediti tramite posta; ∆ 9 - I prodotti THC, ancora illegali a livello federale, non possono. A partire dal 2021, è stato creato o è già stato creato un nuovo settore considerevole, inclusi i franchising.
All'inizio del 2021, "Delta-8"/∆ 8 -THC è uno dei segmenti di prodotti derivati dalla canapa in più rapida crescita.
Problemi di sicurezza
∆ 8 -THC è tipicamente sintetizzato dal cannabidiolo estratto dalla canapa poiché le quantità naturali di Delta 8 presenti nella canapa sono basse. La reazione spesso produce una miscela che contiene altri cannabinoidi e sottoprodotti di reazione sconosciuti. Di conseguenza, la maggior parte dei prodotti venduti come ∆ 8 -THC non sono in realtà puri ∆ 8 -THC. Poco si sa circa l'identità e gli effetti sulla salute delle impurità.
Ricerca
∆ 8 -THC è stato studiato come potenziale trattamento per il glaucoma , le lesioni corneali e la nausea e il vomito indotti dalla chemioterapia (CINV). Uno studio che ha coinvolto un modello murino di disturbo da uso di oppiacei ha scoperto che ∆ 8 -THC ha alleviato alcuni degli effetti fisiologici e comportamentali dell'astinenza da oppiacei. Altri studi su topi e ratti hanno trovato prove di un effetto anticonvulsivante del 8 -THC. Nei ratti, è stato scoperto che 8 -THC riduce i deficit neurologici associati all'encefalomielite autoimmune sperimentale . Gli effetti del ∆ 8 -THC sono stati studiati su un'ampia gamma di tipi cellulari, comprese le cellule di neuroblastoma in coltura e le cellule tumorali orali . Uno studio in silico ha suggerito che ∆ 8 -THC interagisce con il recettore beta degli estrogeni nelle cellule del cancro al seno . Diversi farmaci sperimentali tra cui KM-233 , AM-411 , AM-855 , AMG-36 , AMG-41 , AM-087 , AM-7438 e AMG-3 si basano sulla struttura chimica del ∆ 8 -THC. È stato scoperto che alcuni prodotti della fotoossigenazione del ∆ 8 -THC possiedono attività biologica in vitro.
Sebbene 8 -THC sia un costituente minore della cannabis medica , non sono stati pubblicati grandi studi clinici solo su ∆ 8 -THC per qualsiasi condizione medica a partire dal 2021 secondo il database NIH. Uno studio clinico in Israele che ha coinvolto 108 pazienti affetti da cancro con CINV è stato registrato presso il NIH nel 2005, ma lo studio non è mai stato completato.
Guarda anche
- Cannabinoide
- Cannabis (droga)
- 7,8-diidrocannabinolo
- 11-Idrossi-Delta-8-THC
- delta -3-Tetraidrocannabinolo
- delta -4-Tetraidrocannabinolo
- delta -7-tetraidrocannabinolo ( delta -5-tetraidrocannabinolo)
- delta -10-Tetraidrocannabinolo ( delta -2-tetraidrocannabinolo)
- delta -6-Cannabidiolo
- Esaidrocannabinolo
- Tetraidrocannabinolo
- Tetraidrocannabutolo
- Tetraidrocannabiforolo
- THC-O-acetato
- THC-O-fosfato
- acido ajulemico
- Sistema endocannabinoide


