alfa-amilasi - Alpha-amylase
| alfa-amilasi | |||||||||
|---|---|---|---|---|---|---|---|---|---|

| |||||||||
| Identificatori | |||||||||
| CE n. | 3.2.1.0 | ||||||||
| CAS n. | 9000-90-2 | ||||||||
| Banche dati | |||||||||
| IntEnz | Vista IntEnz | ||||||||
| BRENDA | Ingresso BRENDA | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | Ingresso KEGG | ||||||||
| MetaCyc | passaggio metabolico | ||||||||
| PRIAM | profilo | ||||||||
| Strutture PDB | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
| Dominio catalitico GH13 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Ciclodestrina glucanotransferasi (ec2.4.1.19) (cgtase)
| |||||||||
| Identificatori | |||||||||
| Simbolo | alfa-amilasi | ||||||||
| Pfam | PF00128 | ||||||||
| Clan Pfam | CL0058 | ||||||||
| InterPro | IPR006047 | ||||||||
| SCOP2 | 1ppi / SCOPe / SUPFAM | ||||||||
| Superfamiglia OPM | 117 | ||||||||
| proteine OPM | 1wza | ||||||||
| CAZy | GH13 | ||||||||
| CDD | cd11338 | ||||||||
| |||||||||
| Dominio del foglio beta alfa-amilasi C-terminale | |||||||||
|---|---|---|---|---|---|---|---|---|---|
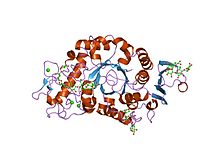 Struttura cristallina di orzo alfa-amilasi isoenzima 1 (amy1) mutante inattivo d180a in complesso con maltoeptaose
| |||||||||
| Identificatori | |||||||||
| Simbolo | Alfa-amile_C2 | ||||||||
| Pfam | PF07821 | ||||||||
| InterPro | IPR012850 | ||||||||
| |||||||||
| Alfa amilasi, dominio all-beta C-terminale | |||||||||
|---|---|---|---|---|---|---|---|---|---|
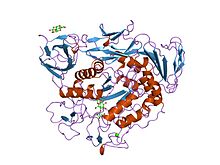 complesso di maltotriosio del mutante della ciclodestrina glicosiltransferasi precondizionata
| |||||||||
| Identificatori | |||||||||
| Simbolo | Alfa-amilasi_C | ||||||||
| Pfam | PF02806 | ||||||||
| Clan Pfam | CL0369 | ||||||||
| InterPro | IPR006048 | ||||||||
| SCOP2 | 1ppi / SCOPe / SUPFAM | ||||||||
| |||||||||
L'alfa-amilasi , (α-amilasi) è un enzima EC 3.2.1.1 che idrolizza i legami alfa di grandi polisaccaridi alfa-collegati , come l' amido e il glicogeno , producendone catene più corte, destrine e maltosio . È la principale forma di amilasi presente nell'uomo e in altri mammiferi. È presente anche nei semi contenenti amido come riserva alimentare ed è secreto da molti funghi. È un membro della famiglia dei glicosidi idrolasi 13 .
Nella biologia umana
Sebbene si trovi in molti tessuti, l'amilasi è più importante nel succo pancreatico e nella saliva , ognuno dei quali ha la propria isoforma di α-amilasi umana. Si comportano diversamente alla focalizzazione isoelettrica e possono anche essere separati nei test utilizzando specifici anticorpi monoclonali . Nell'uomo, tutte le isoforme dell'amilasi si collegano al cromosoma 1p 21 (vedi AMY1A ).
Amilasi salivare (ptyalin)
L'amilasi si trova nella saliva e rompe l' amido in maltosio e destrina . Questa forma di amilasi è anche chiamato "ptialina" / t aɪ əl ɪ n / , che è stato nominato dal chimico svedese Jöns Jacob Berzelius . Il nome deriva dalla parola greca πτυω (sputo), perché la sostanza si ricavava dalla saliva. Romperà grandi molecole di amido insolubili in amidi solubili ( amilodestrina , eritrodestrina e acrodestrina ) producendo amidi successivamente più piccoli e infine maltosio . La ptialina agisce sui legami glicosidici α(1,4) lineari , ma l' idrolisi dei composti richiede un enzima che agisca sui prodotti ramificati. Amilasi salivare è inattivato nello stomaco da acido gastrico . Nel succo gastrico aggiustato a pH 3,3, la ptialina è stata totalmente inattivata in 20 minuti a 37 °C. Al contrario, il 50% dell'attività dell'amilasi è rimasto dopo 150 minuti di esposizione al succo gastrico a pH 4,3. Sia l'amido, substrato della ptialina, sia il prodotto (corte catene di glucosio) sono in grado di proteggerlo parzialmente dall'inattivazione da parte dell'acido gastrico. La ptialina aggiunta al tampone a pH 3.0 ha subito una completa inattivazione in 120 minuti; tuttavia, l'aggiunta di amido a un livello dello 0,1% ha provocato il 10% dell'attività rimanente e un'aggiunta simile di amido a un livello dell'1,0% ha portato a circa il 40% dell'attività rimanente a 120 minuti.
Condizioni ottimali per ptyalin
- pH ottimale – 7.0
- Temperatura corporea umana
- Presenza di alcuni anioni e attivatori:
Variazione genetica nell'amilasi salivare umana
Il gene dell'amilasi salivare ha subito una duplicazione durante l'evoluzione e gli studi di ibridazione del DNA indicano che molti individui hanno ripetizioni multiple in tandem del gene. Il numero di copie del gene è correlato ai livelli di amilasi salivare, misurati mediante analisi di protein blot utilizzando anticorpi contro l'amilasi umana. Il numero di copie geniche è associato all'apparente esposizione evolutiva a diete ad alto contenuto di amido. Ad esempio, un individuo giapponese aveva 14 copie del gene dell'amilasi (un allele con 10 copie e un secondo allele con quattro copie). La dieta giapponese ha tradizionalmente contenuto grandi quantità di amido di riso . Al contrario, un individuo Biaka portava sei copie (tre copie su ciascun allele). I Biaka sono cacciatori-raccoglitori della foresta pluviale che tradizionalmente hanno consumato una dieta a basso contenuto di amido. Perry e colleghi hanno ipotizzato che l'aumento del numero di copie del gene dell'amilasi salivare potrebbe aver migliorato la sopravvivenza in coincidenza con il passaggio a una dieta ricca di amido durante l'evoluzione umana.
Amilasi pancreatica
Pancreatica α-amilasi fende il caso α (1-4) glicosidici di amilosio cedere destrine , maltosio , o maltotriosio . Adotta un meccanismo a doppio spostamento con conservazione della configurazione anomerica . Negli esseri umani, l'amilasi salivare si è evoluta da una sua copia.
In patologia
Il test per l'amilasi è più facile da eseguire rispetto a quello per la lipasi , il che lo rende il test principale utilizzato per rilevare e monitorare la pancreatite . I laboratori medici di solito misurano l'amilasi pancreatica o l'amilasi totale. Se viene misurata solo l'amilasi pancreatica, non si noterà un aumento con la parotite o altri traumi delle ghiandole salivari.
Tuttavia, a causa della piccola quantità presente, il tempismo è fondamentale quando si preleva il sangue per questa misurazione. Il sangue deve essere prelevato subito dopo un attacco di dolore da pancreatite, altrimenti viene escreto rapidamente dai reni .
L'α-amilasi salivare è stata utilizzata come biomarcatore per lo stress e come marcatore surrogato dell'attività del sistema nervoso simpatico (SNS) che non richiede un prelievo di sangue.
Interpretazione
L'aumento dei livelli plasmatici nell'uomo si trova in:
- Trauma salivare (inclusa intubazione anestetica )
- Parotite - causa l'infiammazione delle ghiandole salivari
- Pancreatite – a causa di danni alle cellule che producono amilasi
- Insufficienza renale - a causa della ridotta escrezione
Letture di amilasi totale di oltre 10 volte il limite superiore della norma (ULN) sono indicative di pancreatite. Da cinque a dieci volte l'ULN può indicare una malattia dell'ileo o del duodeno o insufficienza renale, e aumenti inferiori si riscontrano comunemente nella malattia delle ghiandole salivari.
geni
In grano
L'attività dell'α-amilasi nel grano è misurata, ad esempio, dal numero di caduta di Hagberg–Perten , un test per valutare i danni ai germogli, o dal metodo Phadebas . Si verifica nel grano .
Uso industriale
L'α-amilasi viene utilizzata nella produzione di etanolo per rompere gli amidi nei cereali in zuccheri fermentescibili.
Il primo passo nella produzione di sciroppo di mais ad alto contenuto di fruttosio è il trattamento dell'amido di mais con α-amilasi, producendo catene più corte di zuccheri oligosaccaridi .
Un'α-amilasi chiamata "Termamyl", proveniente da Bacillus licheniformis , viene utilizzata anche in alcuni detersivi, in particolare detersivi per piatti e per la rimozione dell'amido.
Vedi amilasi per ulteriori usi della famiglia dell'amilasi in generale.
Potenziale per uso medico
L'α-amilasi ha mostrato efficacia nel degradare i biofilm batterici polimicrobici idrolizzando i legami glicosidici α(1-4) all'interno degli esopolisaccaridi strutturali della matrice della sostanza polimerica extracellulare (EPS).
Inibizione tampone
Si dice che la molecola tris inibisca un certo numero di α-amilasi batteriche, quindi non dovrebbero essere usate nel tampone tris.
Determinazione
Sono disponibili diversi metodi per la determinazione dell'attività dell'α-amilasi e diverse industrie tendono a fare affidamento su metodi diversi. Il test dell'amido iodio, uno sviluppo del test dello iodio , si basa sul cambiamento di colore, poiché l'α-amilasi degrada l'amido ed è comunemente usato in molte applicazioni. Un test simile ma prodotto industrialmente è il test dell'amilasi di Phadebas , che viene utilizzato come test qualitativo e quantitativo in molti settori, come i detersivi, vari alimenti con farina, cereali e malto e la biologia forense.
Architettura di dominio
Le α-amilasi contengono un numero di domini proteici distinti. Il dominio catalitico ha una struttura costituita da un barile alfa/beta a otto filamenti che contiene il sito attivo, interrotto da un dominio legante il calcio di circa 70 aminoacidi che sporge tra il filamento beta 3 e l' alfa elica 3, e un greco carbossi-terminale dominio chiave beta-barile . Diverse alfa-amilasi contengono un dominio beta-sheet, solitamente al capolinea C. Questo dominio è organizzato come un beta-sheet antiparallelo a cinque filamenti. Diverse alfa-amilasi contengono un dominio all-beta, di solito al capolinea C.
Guarda anche
Riferimenti
link esterno
- La proteina alfa-amilasi
- alfa-amilasi presso la National Library of Medicine degli Stati Uniti Medical Subject Headings (MeSH)
