Rilpivirina - Rilpivirine
 | |
 | |
| Dati clinici | |
|---|---|
| Nomi commerciali | Edurant, Rekambys |
| Altri nomi | TMC278 |
| AHFS / Drugs.com | Monografia |
| MedlinePlus | a611037 |
| Dati di licenza | |
Categoria di gravidanza |
|
| Vie di somministrazione |
Per via orale , intramuscolare |
| Codice ATC | |
| Stato legale | |
| Stato legale | |
| Dati farmacocinetici | |
| Legame proteico | 99,7% |
| Metabolismo | CYP3A4 |
| Eliminazione emivita | compresse: 45 ore iniezione: 13–28 settimane |
| Escrezione | 85% tramite feci, 6% tramite urina |
| Identificatori | |
| |
| Numero CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CheBI | |
| ChEMBL | |
| NIAID ChemDB | |
| ligando PDB | |
| Cruscotto CompTox ( EPA ) | |
| Scheda informativa dell'ECHA |
100.224.394 |
| Dati chimici e fisici | |
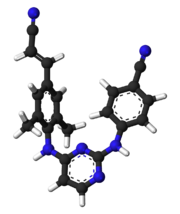
| Formula | C 22 H 18 N 6 |
| Massa molare | 366.428 g·mol −1 |
| Modello 3D ( JSmol ) | |
| |
| |
|
| |
La rilpivirina , venduta con i marchi Edurant e Rekambys , è un farmaco , sviluppato da Tibotec , utilizzato per il trattamento dell'HIV/AIDS . È un inibitore non nucleosidico della trascrittasi inversa (NNRTI) di seconda generazione con maggiore potenza , emivita più lunga e profilo di effetti collaterali ridotto rispetto ai vecchi NNRTI come efavirenz .
Usi medici
Negli Stati Uniti, la rilpivirina è approvata per i pazienti naive al trattamento con una carica virale di 100.000 copie/ml o inferiore all'inizio della terapia. Deve essere combinato con altri farmaci contro l'HIV.
Nell'Unione Europea, rilpivirina è approvata in combinazione con cabotegravir per il trattamento di mantenimento di adulti con livelli di HIV non rilevabili nel sangue (carica virale inferiore a 50 copie/ml) con il loro attuale trattamento antiretrovirale e quando il virus non ha sviluppato resistenza a una certa classe di medicinali anti-HIV chiamati inibitori non nucleosidici della trascrittasi inversa (NNRTI) e inibitori del trasferimento del filamento dell'integrasi (INI).
Moduli disponibili
Il farmaco è disponibile in compresse (marca Edurant ) e come iniezione intramuscolare a lunga durata d'azione da somministrare una volta al mese o ogni due mesi ( Rekambys ). Prima di usare l'iniezione, le compresse vengono somministrate per circa quattro settimane per valutare la tollerabilità.
Controindicazioni e interazioni
Il farmaco è controindicato per l'uso con farmaci che inducono l'enzima epatico CYP3A4 , come carbamazepina , fenitoina , rifampicina ed erba di San Giovanni . Tali farmaci possono accelerare la scomposizione della rilpivirina, diminuendo sostanzialmente le sue concentrazioni plasmatiche e con conseguente potenziale perdita di efficacia e possibile resistenza . Alcuni di questi farmaci inducono anche l'enzima UGT1A1 e quindi riducono le concentrazioni plasmatiche di cabotegravir, compromettendo ulteriormente l'efficacia di questa terapia di associazione.
È anche controindicato in combinazione con inibitori della pompa protonica perché l'aumento del pH gastrico provoca un ridotto assorbimento di rilpivirina dall'intestino, con conseguenze simili a quelle degli induttori del CYP3A4.
Effetti collaterali
Gli effetti indesiderati più comuni della formulazione iniettabile sono reazioni al sito di iniezione (fino all'84% dei pazienti) come dolore e gonfiore, nonché mal di testa (fino al 12%) e febbre o sensazione di calore (nel 10%) . Meno comuni (meno del 10%) sono i disturbi depressivi , l' insonnia e le eruzioni cutanee . Gli effetti collaterali più comuni delle compresse sono anche disturbi depressivi (4,1%), cefalea (3,5%), insonnia (3,5%) ed eruzioni cutanee (2,3%). Tutti questi effetti collaterali si sono verificati durante le terapie combinate di rilpivirina con uno o più altri farmaci contro l'HIV.
Il prolungamento dell'intervallo QT del ritmo cardiaco è stato osservato a dosi molto elevate, ma non è clinicamente rilevante alle dosi standard del farmaco.
Farmacologia
Meccanismo di azione
La rilpivirina è un inibitore non nucleosidico della trascrittasi inversa (NNRTI).
farmacocinetica
Se assunta per via orale, la rilpivirina raggiunge i livelli più alti nel plasma sanguigno dopo circa quattro o cinque ore. L'assunzione del farmaco senza cibo riduce i suoi livelli plasmatici del 40% rispetto all'assunzione con il cibo, che è considerata clinicamente rilevante. Pertanto, si consiglia ai pazienti di assumere il farmaco insieme a un pasto. Dopo l'iniezione nel muscolo, la sostanza raggiunge i livelli plasmatici più elevati dopo tre o quattro giorni.
Indipendentemente dalla modalità di applicazione, la rilpivirina è quasi completamente legata alle proteine plasmatiche (99,7%), principalmente all'albumina . È metabolizzato principalmente dall'enzima epatico CYP3A4 . I metaboliti includono diversi prodotti di ossidazione , glucuronidi e glucuronidi di metaboliti ossidati. L' emivita biologica è di circa 45 ore per le compresse e da 13 a 28 settimane per l'iniezione.
L'eliminazione è stata studiata solo per somministrazione orale: la maggior parte del farmaco viene escreta attraverso le feci (85%), in parte in forma immodificata (25%), in parte sotto forma dei suoi metaboliti (60%). Una quantità minore viene escreta per via urinaria (6%), quasi esclusivamente come metaboliti.

Combinazioni a dose fissa
Un farmaco a dose fissa che combina rilpivirina con emtricitabina e tenofovir disoproxil (TDF) è stato approvato dalla Food and Drug Administration (FDA) statunitense nell'agosto 2011 con il marchio Complera ed è stato approvato per l'uso nell'Unione europea con il marchio Eviplera nel novembre 2011. È stato dimostrato che questa combinazione ha tassi più elevati di fallimento virologico rispetto a emtricitabina/tenofovir/efavirenz nelle persone con carica virale dell'HIV al basale superiore a 100.000 copie/mm 3 .
Un farmaco a dose fissa che combina rilpivirina con emtricitabina e tenofovir alafenamide (TAF) è stato approvato per l'uso negli Stati Uniti nel marzo 2016 con il marchio Odefsey .
Dolutegravir/rilpivirina , venduto con il marchio Juluca, è un farmaco antiretrovirale combinato a dose fissa per il trattamento dell'HIV/AIDS. È stato approvato per l'uso negli Stati Uniti nel novembre 2017 e per l'uso nell'Unione europea nel maggio 2018.
Nel gennaio 2021, la Food and Drug Administration (FDA) statunitense ha approvato cabotegravir/rilpivirina (nome commerciale Cabenuva) per il trattamento delle infezioni da HIV-1 negli adulti per sostituire l'attuale regime antiretrovirale in coloro che sono virologicamente soppressi con un regime antiretrovirale stabile con nessuna storia di fallimento del trattamento e nessuna resistenza nota o sospetta a cabotegravir o rilpivirina. Questo è il primo regime iniettabile completo approvato dalla FDA per adulti con infezione da HIV che viene somministrato una volta al mese. L'etichetta per le compresse di rilpivirina è stata rivista per riflettere le raccomandazioni orali per l'uso con cabotegravir .
Chimica
Come l' etravirina , un NNRTI di seconda generazione approvato nel 2008, la rilpivirina è una diarilpirimidina (DAPY).
Le compresse contengono rilpivirina cloridrato , mentre l'iniezione contiene rilpivirina libera.
Storia
Rilpivirina è entrata negli studi clinici di fase III nell'aprile 2008 ed è stata approvata per l'uso negli Stati Uniti nel maggio 2011 con il marchio Edurant.
Il 15 ottobre 2020, il comitato per i medicinali per uso umano (CHMP) dell'Agenzia europea per i medicinali (EMA) ha adottato un parere positivo, raccomandando il rilascio di un'autorizzazione all'immissione in commercio per rilpivirina con il nome commerciale Rekambys, destinato al trattamento delle malattie umane infezione da virus dell'immunodeficienza di tipo 1 (HIV-1) in combinazione con l' iniezione di cabotegravir . È stato approvato per uso medico nell'Unione Europea nel dicembre 2020. I due farmaci sono i primi antiretrovirali in una formulazione iniettabile a lunga durata d'azione. Ciò significa che invece delle pillole giornaliere, le persone ricevono iniezioni intramuscolari mensilmente o ogni due mesi.
Riferimenti
link esterno
- "Rilpivirina" . Portale informativo sui farmaci . Biblioteca nazionale di medicina degli Stati Uniti.
- "Rilpivirina cloridrato" . Portale informativo sui farmaci . Biblioteca nazionale di medicina degli Stati Uniti.
