Lipossina - Lipoxin
|
|
| nomi | |
|---|---|
|
Nome IUPAC preferito
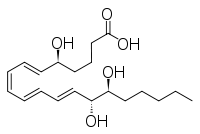
(5 S ,6 E ,8 Z ,10 E ,12 E ,14 R ,15 S )-5,14,15-acido triidrossiicosa-6,8,10,12-tetraenoico |
|
| Altri nomi
LXB4
|
|
| Identificatori | |
|
Modello 3D ( JSmol )
|
|
| CheBI | |
| ChemSpider | |
|
PubChem CID
|
|
|
|
|
|
| Proprietà | |
| C 20 H 32 O 5 | |
| Massa molare | 352.46508 g/mol |
|
Salvo indicazione contraria, i dati sono forniti per i materiali nel loro stato standard (a 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Riferimenti alla casella informativa | |
Una lipossina ( LX o Lx ), acronimo di prodotto di interazione lipossigenasi , è un metabolita autacoide bioattivo dell'acido arachidonico prodotto da vari tipi di cellule. Sono classificati come eicosanoidi non classici e membri della famiglia dei mediatori pro-risoluzione specializzati (SPM) dei metaboliti degli acidi grassi polinsaturi (PUFA). Come altri SPM, gli LX si formano durante e quindi agiscono per risolvere le risposte infiammatorie . Inizialmente, sono state identificate due lipossine, lipossina A 4 (LXA 4 ) e LXB 4 , ma studi più recenti hanno identificato epimeri di questi due LX: le epi-lipossine , 15-epi-LXA 4 e 15-epi-LXB 4 rispettivamente.
Storia
LXA 4 e LXB 4 sono stati descritti per la prima volta da Serhan, Hamberg e dal premio Nobel Samuelsson nel 1984. Hanno riferito che i neutrofili del sangue umano , quando stimolati, producono queste due lipossine e che i neutrofili, quando stimolati da uno degli LX, montano l' anione superossido (O 2 − ) Risposte di generazione e degranulazione . Entrambe le risposte sono considerate pro-infiammatorie in quanto, mentre mirano a neutralizzare i patogeni invasori e a digerire il materiale estraneo, possono contribuire a danneggiare i tessuti ospiti e quindi a prolungare e promuovere un'ulteriore infiammazione. Studi successivi, tuttavia, hanno scoperto che queste lipossine, così come i loro epimeri, epi-LXA 4 e LXB 4 , agiscono principalmente per smorzare e risolvere l'infiammazione, ovvero sono agenti di segnalazione cellulare anti-infiammatori .
Biochimica
Le lipossine sono derivate enzimaticamente dall'acido arachidonico , un acido grasso ω-6 . Strutturalmente, sono definiti come metaboliti dell'acido arachidonico che contengono tre residui idrossilici (detti anche residui idrossilici) e quattro doppi legami . Questo distingue strutturali definizione dalle altre SPM quali le resolvine , neuroprotectins e maresins , che sono metaboliti del omega 3 acidi grassi , acido eicosapentaenoico o acido docosaesaenoico , nonché una serie di metaboliti derivati da altri PUFA (vedi pro- specializzata mediatori risolutivi ). Tutti questi altri SPM hanno attività e funzioni simili, anche se non necessariamente identiche, alle lipossine.
Sintesi
La formazione di LX è conservata in un'ampia gamma di specie animali, dai pesci all'uomo. La biosintesi degli LX richiede due attacchi enzimatici separati all'acido arachidonico (AA). Un attacco comporta l'attaccamento di un residuo idroperossi (-O-OH) al carbonio 15, la conversione di questa specie in un 14,15- epossido e la risoluzione di questo epossido per formare 14,15-diidrossi-eicosatetraenoato o 15-idrossi -prodotti eicosatraenoato. Questo passaggio è catalizzato da enzimi con attività 15-lipossigenasi che nell'uomo include ALOX15 , ALOX12 , cicloossigenasi 2 trattata con aspirina e citocromo P450 delle sottoclassi microsomiali, mitocondriali o batteriche. ALOX15B può anche condurre questo metabolismo. L'altro punto di attacco dell'enzima forma un 5,6- epossido che viene risolto in prodotti 5,6-diidrossi-eicosatetraenoato o 5-idrossi-eicosatetraenoato; questo passaggio catalizzato dalla 5-lipossigenasi (ALOX5). Di conseguenza, queste doppie ossigenazioni producono 5,6,15-triidrossi- o 5,14,15-triidrossi-eicosatetraenoati. Le doppie ossigenazioni possono essere condotte all'interno di un unico tipo cellulare che possiede ALOX5 e un enzima con attività 15-lipossigenasi o, in alternativa, da due diversi tipi cellulari, ognuno dei quali possiede una di queste attività enzimatiche. In quest'ultima via biosintetica transcellulare , un tipo di cellula forma il 5,6-diidrossi-, 5-idrossi, 14,15-diidrossi- o un 15-idrossi-eicosatetraenoato, e poi passa questo intermedio a un secondo tipo di cellula, che lo metabolizza nel prodotto finale LX. Ad esempio, gli LX sono formati da piastrine che, in mancanza di ALOX5, non sono in grado di sintetizzarli. Piuttosto, i neutrofili formano il 5,6-epossido, leucotriene A4 (LTA 4 ), tramite ALOX5 e lo passano alle piastrine che poi lo riducono a prodotto 5,6-diidrossi-eicosateteraenoato e lo metabolizzano ulteriormente attraverso ALOX12 per formare il 15- prodotto idrossilico, LXA 4 . I due LX si distinguono dai loro epimeri 15-epi-LTX per le loro formule strutturali:
- LxA 4 : 5 S ,6 R ,15 S -triidrossi-7 E ,9 E ,11 Z ,13 E -acido eicosatetraenoico
- LxB 4 : 5 S ,14 R ,15 S -triidrossi-6 E ,8 Z ,10 E ,12 E -acido eicosatraenoico
- 15-epi-LxA 4 : 5 S ,6 R ,15 R -triidrossi-7 E ,9 E ,11 Z ,13 E -acido eicosatetraenoico
- 15-epi-LxB 4 : 5 S ,14 R ,15 R -triidrossi-6 E ,8 Z ,10 E ,12 E -acido eicosatrienoico
Si noti che i due LX hanno i loro residui 15-idrossilici nella configurazione di chiralità S perché tutti gli enzimi ALOX formano prodotti 15 S- idrossi AA. Al contrario, i residui 15-idrossi delle due epi-LX sono prodotti della chiralità 15 R perché sono sintetizzati dalla cicloossigenasi 2 trattata con aspirina o dai citocromi P450 microsomiali, mitocondriali o batterici ; questi enzimi formano quasi interamente o in parte 15 R- prodotti idrossilici. (15-Epi-LTA4 4 e 15-epi-LTB4 4 sono talvolta denominati AT-LxA 4 e AT-LxB 4 , rispettivamente, quando riconoscono la loro formazione da parte della cicloossigenasi 2 trattata con aspirina, cioè da una cicloossigenasi 2 attivata da una spirin- T rigger. )
Oltre alle vie citate sopra, è stato dimostrato che altre vie metaboliche transcellulari producono LX. Ad esempio, 5-lipossigenasi (cioè (ALOX5) nei neutrofili e 15-lipossigenasi -1 (cioè ALOX15) negli eritrociti e reticolociti immaturi operano in serie per formare LxA4 4 e LxB4 4 ; questo percorso si verifica anche nelle interazioni seriali tra neutrofili ed eosinofili tra epitelio o M2 Macrofagi /monociti e neutrofili e endotelio o muscolo scheletrico e neutrofili.
Stimolazione della sintesi
Le lipossine si formano comunemente come conseguenza della stimolazione della produzione di metaboliti pro-infiammatori dell'acido arachidonico. Tuttavia, alcune citochine come IFN-γ e IL-1β aumentano ulteriormente la produzione di lipossine (così come di altri metaboliti e proteine PUFA anti-infiammatori, ad esempio IL4 .
Ulteriore metabolismo
Gli LX sono rapidamente metabolizzati, principalmente dai macrofagi, a prodotti inattivi venendo ossidati al carbonio 15 per formare prodotti LX 15- cheto (chiamati anche 15-oxo) da una deidrogenasi 15-idrossiprostaglandina ; 15-oxo-LXA 4 può essere ulteriormente metabolizzato a 13,14-diidro-LXA 4 da un'ossidoreduttasi . 15-Epi-LXA 4 e 15-epi-LXB 4 sono più resistenti all'enzima di deidrogenazione rispetto ai loro epimeri LX. In conseguenza del funzionamento di questa via anabolica , gli LX hanno emivite molto brevi in vivo , gli epi-LX hanno emivite in vivo più lunghe e quindi potenze maggiori rispetto ai loro epimeri LX e lipossine sintetiche che sono metabolicamente resistenti a questa via sono stati preparati, utilizzati in modelli animali per studiare le attività di LX e testati come potenziali agenti terapeutici negli animali e nell'uomo.
Simile a vari altri metaboliti AA come LTA4 e acido 5-osso-eicosatetraenoico , cellule e tessuti possono convertire gli LX in prodotti 20-idrossi mediante l' ossidazione degli omega ; hanno anche dimostrato di legare LXA 4 al glutatione per formare cisteinil-lipossine , inizialmente LXC 4 , che viene poi metabolizzato in sequenza in LXD 4 e LXE 4 . Il ruolo di queste vie nel limitare o contribuire all'attività degli LX non è stato completamente valutato.
Sistema endocannabinoide
Si trova che il lipide antinfiammatorio Lipoxin A 4 è un endogena allosterico potenziatore CB1 recettore cannabinoide . Lipoxin A 4 migliorare l'affinità di anandamide a questo recettore di esercitare effetti cannabimimetica nel cervello , migliorando allostericamente segnalazione AEA e quindi potenziare gli effetti di questo endocannabinoidi sia in vitro e in vivo . In aggiunta a questo, Lipoxin A 4 mostra una CB1 dipendente dal recettore effetto protettivo contro β-amiloide indotta memoria spaziale compromissione nei topi.
Analoghi della lipossina
Relativamente stabili, cioè metabolicamente resistenti, analoghi sintetici di LX e 15-epi-LXA 4 s innescati dall'aspirina possono imitare molte delle desiderabili azioni antinfiammatorie e "pro-risoluzione" degli LX nativi e sono in fase di test per l'uso clinico. Strutturalmente, questi analoghi LX spesso imitano gli LX nell'essere o nell'assomigliare molto a un acido grasso triidrossilico a 20 atomi di carbonio, ma sono resistenti all'inattivazione metabolica della 15-idrossiprostaglandina deidrogenasi avendo una modifica strutturale ingombrante o di altro tipo vicino ai loro residui 15-idrossi. Ad esempio, alcuni analoghi alterano semplicemente la struttura di un LX: sostituendo un atomo di idrogeno con un residuo di metile al carbonio 15 su LXA 4 per formare 15-metil-LXA 4 ; cambiando gli ultimi 4 atomi di carbonio di LXA 4 o 15-epi-LXA 4 in un residuo 1-fenossi o residuo 1-fenossi-4-fluoro per formare 16-fenossi-LX 4 , 15-epi-15-fenossi-LXA 4 , 16-(para-fluoro-fenossi-LXA 4 , o 15-epi-16-(para-fluoro-fenossi-LXA 4 ; e formando un legame tra il carbonio 9 e il carbonio 14 di LXA 4 per formare un analogo dell'anello fenilico interno chiamato aromatico LXA 4 ; altri analoghi strutturali più complessi in fase di sviluppo includono analoghi 15-epi-LXA 4 denominati ZK-142 e ZK994.
Attività biologica
Studi cellulari
Nelle fasi iniziali di molte risposte infiammatorie acute, i tessuti danneggiati, gli agenti patogeni invasori e altri eventi locali fanno sì che le cellule vicine producano e rilascino metaboliti pro-infiammatori derivati dall'acido arachidonico come: leucotrieni (LT), ad esempio LTB 4 , LTB 4 , LTC 4 , LTD 4 , LTE e 4 ; acidi idrossieicosatetraenoici (HETE), ad esempio 5-HETE e 12-HETE ; e oxoeicosanoidi (oxo-ETE), ad esempio acido 5-osso-eicosatetraenoico (5-oxo-ETE) e 12-oxo-ETE. Questi metaboliti procedono ad agire direttamente o indirettamente per reclutare leucociti circolanti, macrofagi tissutali e cellule dendritiche tissutali nel sito del tessuto disturbato. La conseguente congregazione dei vari tipi cellulari favorisce le vie transcellulari nella formazione di mediatori pro- risolvinti (SPM) specializzati, compresi gli LX, che procedono poi a stimolare le risposte cellulari e tissutali che tendono ad invertire le azioni dei mediatori pro-infiammatori, smorzare e invertire la risposta infiammatoria e avviare la riparazione dei tessuti.
LXA 4 e 15-epi-LXA 4 sono ligandi del recettore ad alta affinità e attivatori del recettore FPR2 . FPR2, che ora è chiamato recettore ALX, ALX/FPR o ALX/FPR2, è un recettore accoppiato a proteine G inizialmente identificato come recettore per il fattore chemiotattico dei leucociti , N-formilmetionina-leucil-fenilalanina (FMLP), in base alla sua somiglianza della sequenza di amminoacidi con il noto recettore FMLP , FPR1 . Almeno sei omologhi di questo recettore si trovano nei topi. ALX/FPR è un recettore promiscuo (cioè che interagisce con diversi ligandi) che si lega ed è attivato da altri ligandi tra cui: a) vari oligopeptidi N-formil che, come FMLP, sono rilasciati da microbi e mitocondri o sono analoghi di quelli rilasciati da microbi e mitocondri; b) oligopeptidi non formil-derivati da microbi; c) alcuni polipeptidi che sono associati allo sviluppo di amiloidosi cronica e/o infiammazione comprese le proteine dell'amiloide sierica A (SAA), un peptide di 42 amminoacidi beta-amiloide chiamato Aβ42, Humanin e un frammento solubile scisso (aminoacidi 274 -388) dal recettore dell'urochinasi ; e d) altri SPM tra cui Resolvins RvD1, RvD2, RvD5, AT-RvD1 e RvD3 (vedi mediatori specializzati pro-risoluzione ).
LXA 4 e 15-epi-LXA 4 inibiscono la chemiotassi , la trasmigrazione , la generazione di superossido, l' attivazione di NF-κB e/o la generazione di citochine pro-infiammatorie (ad es. IL8 , IL13 , IL12 e IL5 ) da parte di neutrofili, eosinofili, monociti , innata cellule linfoidi e / o macrofagi , nonché proliferazione suppress e produzione di IgM e IgG anticorpi da linfociti B . Queste azioni sembrano coinvolgere la stimolazione delle vie di segnalazione antinfiammatorie, ma anche il blocco delle azioni di altri ligandi ALX/FPR che simulano le vie proinfiammatorie. I topi transgenici fatti per sovraesprimere ALX/FPR mostrano risposte infiammatorie notevolmente ridotte a diversi insulti. LXA 4 e 15-epi-LXA 4 , quando introdotti per somministrazione intratecale nei roditori, sopprimono la percezione del dolore infiammatorio; questa azione può coinvolgere il recettore ALX/FPR dimostrato essere presente sugli astrociti spinali dell'animale da esperimento e, sulla base di studi che utilizzano 15-epi-LXA, l'inibizione del complesso di segnalazione dell'inflammasoma NALP1 .
Con meccanismi ancora da identificare chiaramente, i due LX inoltre: a) stimolano la capacità di uccidere i batteri dei leucociti e delle cellule epiteliali delle vie aeree; b) bloccare la produzione della citochina pro-infiammatoria, TNFα , mentre aumenta la produzione della citochina anti-infiammatoria, CCR5 da parte dei linfociti T ; c)' potenziare la capacità dei monociti e dei macrofagi di fagocitare (cioè ingerire) e quindi rimuovere i neutrofili apoptotici e gli eosinofili potenzialmente dannosi dai siti infiammatori (vedi Efferocitosi ) sia attraverso l'effetto diretto di queste cellule sia stimolando le cellule NK a farlo; d) indurre vari tipi di cellule a ridurre la produzione di specie reattive dell'ossigeno proinfiammatorie e l'espressione di molecole di adesione cellulare e aumentare la produzione dell'inibitore piastrinico, PGI2 e del vasodilatatore, ossido nitrico ; e) inibire la produzione di citochine proinfiammatorie da parte delle cellule mesangiali , fibroblasti e altri tipi di cellule proinfiammatorie ; e f) ridurre la percezione del dolore dovuto all'infiammazione.
LXA 4 e 15-epi-LTA 4 agiscono anche mobilitando fattori di trascrizione che regolano l'espressione di vari geni regolatori dell'infiammazione. LXA 4 stimola vari tipi di cellule a promuovere l'ingresso di Nrf2 nel nucleo e quindi ad aumentare l'espressione di geni come l' eme ossigenasi-1 (HMOX1), che aumenta la produzione dell'agente di segnalazione gassoso antinfiammatorio, monossido di carbonio e geni coinvolto nella sintesi del glutatione , un prodotto che neutralizza lo stress ossidativo e il danno tissutale indotto dall'ossidazione. Gli analoghi strutturali metabolicamente resistenti di LXB 4 e 15-epi-LXA 4 inibiscono la formazione di perossinitrito (cioè ONOO − ) per attenuare la mobilitazione dei fattori di trascrizione NFκB e AP-1 riducendo il loro accumulo nel nucleo di neutrofili, monociti e linfociti; NFκB e AP-1 aumentano l'espressione dei geni pro-infiammatori. I due LXB innescano anche l'attivazione del soppressore delle proteine di segnalazione delle citochine (vedi proteine SOCS ) che, a loro volta, inibiscono l'attivazione dei fattori di trascrizione della proteina STAT che up-regolano molti geni che producono prodotti pro-infiammatori.
LXA 4 e 15-epi-LXA 4 sono anche antagonisti ad alta affinità del recettore 1 del cisteinil leucotriene per il quale i leucotrieni (LT) LTC4 , LTD4 e LTE4 sono agonisti , ovvero i tre leucotrieni si legano e quindi stimolano la contrazione della muscolatura liscia, chemiotattassi degli eosinofili , secrezione di ghiandole mucose e varie altre risposte pro- allergiche nelle cellule del polmone, della pelle e di altri tessuti. (CysLT1 e ATX/FPR2 hanno un'identità di sequenza amminoacidica del 47%.) La capacità di questi LX di bloccare le azioni dei tre LT può contribuire alla loro capacità di risolvere le reazioni allergiche; per esempio, LXA4 rilassa la contrazione della muscolatura liscia causata dai cisteinil leucotrieni nel test della tasca guancia del criceto e un analogo 15-epi-LXAA 4 metabolicamente resistente inibisce potentemente l' ipersensibilità e l'infiammazione delle vie aeree guidate da allergeni in un modello murino.
A concentrazioni più elevate (> 30 nmole / litro), LXA 4 si lega al AHR , il recettore arylhydrocarbon; in seguito a questo legame, AHR entra nel nucleo, dove si unisce al traslocatore nucleare AhR (ARNT). Il complesso AHR/ARNT si lega agli elementi di risposta xenobiotici per attivare la trascrizione dei geni, la maggior parte dei quali è coinvolta principalmente nel metabolismo xenobiotico. Questi geni includono SOCS2 (ovvero soppressore del segnale delle citochine 2), CYP1A1 , CYP1A2 , CYP1B1 , subunità Ya della glutatione S-transferasi , chinone ossidoreduttasi, UDP-glucuronosiltransferasi e famiglia dell'aldeide deidrogenasi 3, membro A1 . Questa attività di LXA 4 è stata dimostrata solo nelle cellule murine.
LXA 4 si lega e attiva il recettore alfa degli estrogeni . In questa capacità, imita una molecola estrogenica per stimolare le cellule epiteliali dell'endometrio umano in vitro e il tessuto uterino di topo in vivo .
Le azioni di LXB 4 e 15-epi-LXB 4 sono state molto meno definite di quelle dei loro analoghi LXA 4 . Il loro meccanismo di stimolazione delle cellule bersaglio (ad esempio i recettori) non è noto. È stato dimostrato che uno o entrambi questi analoghi inibiscono il reclutamento dei neutrofili nei siti di infiammazione, inibiscono la citotossicità delle cellule NK , stimolano il reclutamento di monociti nei siti infiammatori, migliorano la fagocitosi dei macrofagi e sopprimono la percezione del dolore infiammatorio nei roditori.
Studi su modelli animali
Infiammazione non infettiva
È stato dimostrato che una o più lipossine o i loro analoghi metabolicamente resistenti sopprimono, limitano la gravità e/o aumentano la sopravvivenza in un'ampia gamma di malattie infiammatorie e allergiche, come valutato in studi su modelli murini e ratti. Questi studi includono modelli di evocati sperimentalmente: Endometriosi , colite , peritonite ; pancreatite ; infiammazione renale e glomerulonefrite ; asma polmonare , danno polmonare indotto da acido, fibrosi cistica , pleurite , infiammazione cerebrale e componente infiammatoria del morbo di Alzheimer ; lesioni vascolari da ischemia-riperfusione a vari organi compreso il cuore e l'arto posteriore; allografo rigetto del trapianto di cuore, rene e midollo osseo ; artrite ; dermatite ; parodontite ; infiammazione della cornea ; e dolore e iperalgesia basati sull'infiammazione .
Le lipossine hanno effetti protettivi in modelli animali di infiammazione basata su infezione: a) LXA 4 e un analogo di LXA 4 hanno ridotto l'infiammazione sistemica e migliorato la sopravvivenza in modelli di ratto di sepsi batterica Gram-negativa ; b) 15-epi-LXA 4 ha soppresso il danno polmonare (cioè, shock polmonare o sindrome da distress respiratorio acuto ) causato dall'iniezione intraperitoneale di Escherichia coli nei topi; c) topi transgenici resi carenti nella sintesi della lipossina mediante delezione del loro gene Alox5 erano più suscettibili agli effetti infiammatori e letali di Toxoplasma gondii e sono stati salvati da questi difetti da LXA4 4 ; d) LXA 4 ha ripristinato la funzione macrofagica causata dal virus respiratorio sinciziale in topi transgenici carenti della sintesi della lipossina dalla delezione del gene Alox5 ; e) LXA 4 ha migliorato la parodontite infettiva in modelli di coniglio e suino. f) 15-epi-LXA 4 ha diminuito i livelli ematici del parassita, ridotto l'infiammazione cardiaca e aumentato la sopravvivenza in un modello murino di malattia di Chagas indotta da Trypanosoma cruzi ; f)' 15-epi-LXA 4 sopravvivenza prolungata in un modello murino di malaria cerebrale indotta da Plasmodium berghei ; e g) LXA 4 riduce la durata della risposta allergica all'infestazione parassitaria, Angiostrongylus costaricensis .
Tuttavia, le lipossine hanno anche effetti dannosi in questi modelli: l'infezione da aerosol con Mycobacterium tuberculosis in topi transgenici difettosi in ALOX5, che contribuisce alla sintesi di LX, ha mostrato un'infiammazione molto meno grave e una migliore sopravvivenza rispetto ai topi di controllo; e il trattamento dei topi transgenici con LXA 4 orale ha invertito l'effetto protettivo della delezione di ALOX5.
Studi umani
Studi preclinici
LX ed epi-LX sono stati rilevati in vari tessuti umani sottoposti a un'ampia gamma di reazioni infiammatorie, reazioni allergiche e altre condizioni come nel sangue di pazienti sottoposti ad angioplastica coronarica o esercizio fisico intenso. LXA 4 inibisce l'azione di contrazione bronchiale di LTC4 e rilassa i bronchi precontratti negli individui asmatici.
L'herpesvirus associato al sarcoma di Kaposi (KSHV) provoca la trasformazione maligna delle cellule umane ed è responsabile del sarcoma di Kaposi e del linfoma da versamento primario , due tumori che affliggono in particolare gli esseri umani infettati dall'HIV . Gli studi nel sarcoma di Kaposi umano e nelle cellule di linfoma a versamento primario hanno scoperto che: a) KSHV promuove la produzione di citochine pro-infiammatorie, lipossigenasi, cicloossigenasi e metaboliti delle ultime due classi di enzimi mentre sopprime la produzione di agenti di segnalazione antinfiammatori come LXA 4 , apparentemente come una strategia per promuovere la sua latenza e capacità di trasformazione maligna; b)' Le cellule del sarcoma di Karposi e del linfoma da versamento primario esprimono il recettore ALX/FPR; e c)' il trattamento di queste ultime cellule con LXA 4 o 15-epi-LXA 4 inverte questo profilo pro-malignità della segnalazione pro-infiammatoria mediante un meccanismo ALX/FPR-dipendente. Questi studi suggeriscono che i due LX oi loro analoghi dovrebbero essere testati in modelli animali per determinare se potrebbero essere utili per il trattamento dei due tumori maligni umani.
Studi clinici
In uno studio controllato randomizzato , l'applicazione topica di 15-epi-LXA4 o un analogo relativamente stabile di LXB4, 15 R/S -metil-LXB4, ha ridotto la gravità dell'eczema in uno studio su 60 neonati.
Attualmente, BLXA4, un analogo della lipossina, è in fase di sperimentazione clinica 1 e attualmente sta reclutando volontari per il trattamento della gengivite orale (vedi: Sicurezza ed efficacia preliminare dell'analogo della lipossina BLXA4-ME Risciacquo orale per il trattamento della gengivite (BLXA4) su https:// Clinicaltrials.gov/ct2/show/NCT02342691?term=Lipoxin&rank=3 ).
Guarda anche
Riferimenti
link esterno
- Lipossine presso la National Library of Medicine degli Stati Uniti Medical Subject Headings (MeSH)

